- Research article
- Open Access
- Published: 21 May 2009
- Alexandra Peyser1,
- Jacob Rube1,
- Freya Tarapore1,
- Rachel Frank1,
- Suzanne Vento1,
- Cathy Hoffman1,
- Elsa Valderrama2,
- Douglas Charney2,
- Beatrice Goilav1 &
- …
- Howard Trachtman1
BMC Nephrology
volume 10, Article number: 11 (2009)
Cite this article
-
8143 Accesses
-
15 Citations
-
Metrics details
Abstract
Background
Previous studies have examined the spectrum of diseases identified with a kidney biopsy and the complications of the procedure. However, few studies have examined the utility of the test to clarify the diagnosis and guide treatment of pediatric patients. This retrospective, single-center chart review was performed to test the hypothesis that at least 80% of native kidney biopsies provide clinically valuable information that rationally guides diagnosis and patient management.
Methods
200 biopsies performed between January 1, 2000 and June 30, 2008 were reviewed. A scheme composed of six categories was devised to classify the utility of each kidney biopsy.
Results
196 complete case files were available for review. Twenty-four (12.2%) biopsies did not shed light on the diagnosis and were unhelpful in patient management – 21 biopsies (10.7%) were non-diagnostic and 3 (1.5%) failed to yield enough tissue for examination. The number of unhelpful biopsies did not cluster in any specific disease entity.
Conclusion
Our findings provide guidance to nephrologists about the total risk of a kidney biopsy, including uninformative results, when seeking informed consent for the procedure. The results suggest an appropriate balance has been reached which maximizes the use of kidney biopsies while minimizing the risk of this invasive procedure (word count: 202).
Peer Review reports
Background
A kidney biopsy is an important diagnostic procedure in nephrology and can aid in determining the appropriate diagnosis, treatment, and prognosis for specific patients. Based upon physical examination, urinalysis and blood tests, physicians attempt to make a clinical diagnosis which is used to guide treatment. This is not always feasible using non-invasive tools, and in such cases a kidney biopsy may need to be performed to confirm or determine the diagnosis, severity, and urgency of therapy.
A kidney biopsy may not always provide information that is needed or pertinent to the clinical scenario. Sometimes an adequate tissue sample of the kidneys cannot be obtained or the information provided from the biopsy fails to shed any light on the patients’ symptoms or clinical data. Due to the invasiveness of the procedure, it is important, when recommending a biopsy for an individual patient, to bear in mind not only the risks of the procedure itself but the distinct possibility that it might prove unhelpful in the patient’s management.
There are a number of recent studies that have detailed the array of diagnoses obtained from kidney biopsies in adults [1–8] and children [9–13] with renal disease. Other reports have assessed the clinical impact that a biopsy may have, but they focused primarily on the risk factors and resulting complications of performing renal biopsies [4]. In this study, we defined a novel system that enabled us to ascertain the usefulness of a particular biopsy by analyzing predictions of the diagnosis pre-biopsy and the physician’s treatment decision post biopsy. Using this scheme, we tested the hypothesis that at least 80% of native kidney biopsies provided clinically valuable information that rationally guided the formulation of the patient’s prognosis and treatment.
Methods
Patients
A database of biopsy procedures was obtained from the Department of Pathology that contained information on all native kidney biopsies completed at Schneider Children’s Hospital between January 1, 2000 and June 31, 2008. The database included the patient’s name, date of biopsy, date of birth, and final diagnosis.
The medical records of patients were retrieved from active clinical files or from off-site storage. The following data were extracted from each available chart: age, gender, blood pressure, dipstick urinalysis results, height (cm), serum creatinine, estimated glomerular filtration rate (GFRe), and urine protein/creatinine ratio in an early morning specimen at the last evaluation prior to the biopsy. In addition, the reason for biopsy, physician’s predicted diagnosis, the biopsy-confirmed diagnosis, and treatment outcome were recorded. The predicted diagnosis was based on the correspondence from the nephrologist who performed the biopsy to the patient’s primary physician or was based on the clinical diagnosis recorded on the biopsy report at the time of submission of the tissue sample.
Classification of diagnostic outcomes of the biopsy: A six-point scheme was designed to determine whether the biopsy served as a useful tool in establishing treatment. If the physician conclusively predicted a particular diagnosis which the biopsy confirmed, the patient was categorized as type 1. A type 2 categorization denoted a biopsy that confirmed one of multiple possible diagnoses. A type 3 categorization accounted for an incorrect pre-biopsy prediction but in which the biopsy finding was conclusive and sufficient to determine appropriate treatment. If the biopsy was used to determine the severity of an established disease, category 4 was assigned to that patient. Failures were identified as either content based or technical and were separated accordingly. Thus, patients in whom the biopsy was insufficient on its own to define prognosis and treatment were categorized as type 5. Technical failures, namely an inability to obtain tissue, were categorized as type 6.
Each case was independently reviewed by one of the four primary authors (AP, JR, BS, FT). Clinical and biopsy reports were recorded and categorized according to the scheme outlined above. Agreement between all pairs of primary reviewers was reached in over 85% of all cases. When there was a discrepancy between the primary reviewers, an independent observer (RF), who did not perform the biopsy, reviewed the case. This reviewer also checked randomly selected charts for accuracy and agreed with the primary reviewers in all cases. A nurse was chosen to adjudicate conflicts among the primary reviewers and to confirm accuracy of the chart reviews because this person would be less likely to be biased in interpreting the utility of the kidney biopsy procedures. The nephrologist who did the kidney biopsy did not participate in the categorization of the informational outcome of the procedure to avoid potential bias.
Statistical Methods
Data are reported as mean ± SD. Differences in proportion were assessed by the chi square or Fisher exact test as appropriate. Differences were considered statistically significant if the P value was <0.05. All information was gathered on a pre-approved form.
Data were de-identified and coded by study number in accordance with the Health Insurance Portability and Accountability Act guidelines (HIPAA). This chart review was approved by the Institutional Review Board of North Shore-LIJ Health System.
Results
A total of 200 biopsies were identified in the pathology database. All charts were retrieved. 4 charts were excluded because the biopsy was done at a different center and the diagnostic assessment and its impact on management by the attending physician could not be directly assessed. Thus, this report is based on the outcomes of 196 kidney biopsies.
The number of biopsies per year is illustrated in Figure 1 which demonstrates a fairly steady rate of performance of this procedure. The vast majority, 183 out of 196 (93%), of the procedures were performed in the outpatient setting. The hospitalized patients represented the cohort in which a kidney biopsy was done to assess acute renal dysfunction. The clinical characteristics of the patients are summarized in Table 1. Of note, 77 (59%) of the patients had UP/C >1 and 30 (15%) had GFRe <90 mL/min/1.73 m2.
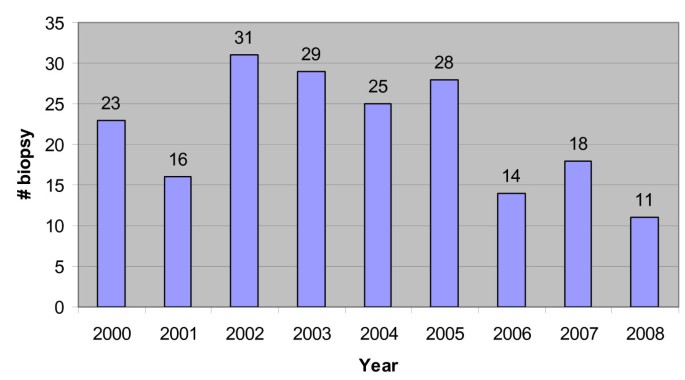
This graph illustrates the annual number of biopsies during the study period, 01/2000 – 06/2008.
Full size image
Full size table
Eleven of the patients who had biopsies underwent repeat biopsies. Nine patients had a second biopsy, one had three, and another underwent four procedures. In the last case, of the four biopsies performed, one of the biopsies was a technical failure. In two of these patients, the first biopsies were normal or non-diagnostic and subsequent biopsies showed FSGS and MPGN, respectively. In two other patients, neither the original nor follow up biopsies resulted in a definitive diagnosis. In the remaining 6 patients, the repeat kidney biopsy was done to assess response to treatment, 4 in patients with SLE and 2 in patients with MPGN.
Fifty-eight (29%) patients were classified as type 1, 28 (15%) were type 2, 27 (14%) were type 3, 59 (30%) were type 4 (Figure 2). Of the unsuccessful biopsies, 21 (10.7%) of the biopsies were inconclusive and further testing was required to confirm a diagnosis (type 5). In 3 of these cases, treatment was based upon the clinical findings rather than the histopathological diagnosis reported after the biopsy. In the remaining 18 cases, 5 patients were started on non-immunosuppressive, renoprotective treatment, 8 were followed without initiation of any disease-specific therapy, and 5 were lost to follow-up or transferred to internal medicine nephrology services for further care. Therefore, these biopsies were considered unhelpful. Finally, 3 (1.5%) biopsies failed to yield adequate tissue samples (type 6).
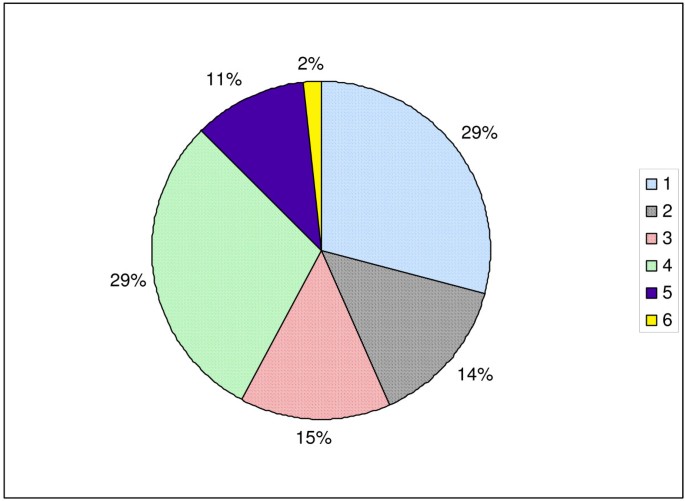
Category 1: Predicted diagnosis confirmed
Category 2: One of several predicted diagnoses confirmed
Category 3: Unexpected but treatable diagnosis made
Category 4: Assessment of disease severity Category 5: Non-diagnostic
Category 6: Technical failure
This graph illustrates the diagnostic categories for the 196 biopsies with complete information that were reviewed. Note that the values for percentage in the pie chart have been rounded off to whole numbers. 1, a biopsy that revealed the specific diagnosis predicted by the physician; 2, a biopsy that confirmed one of multiple possible diagnoses; 3, a biopsy that revealed disease that was different than the pre-biopsy prediction but which was conclusive and sufficient to determine appropriate treatment; 4, a biopsy done to determine the severity of an established disease; 5, a biopsy that was insufficient on its own to define prognosis and treatment; 6, a biopsy that was a technical failure with inability to obtain tissue.
Full size image
The diagnostic utility of the kidney biopsies based on the pre-biopsy diagnosis is summarized in Table 2. The percentage of diagnostically failed biopsies ranged from 0 to 33%. However, focusing on diagnostic entities that contained ≥ 10 patients, there were no significant differences in the rate of this problem for any specific clinical entity.
Full size table
Discussion
In this review, useful biopsies were defined as those that definitively established the diagnosis and which provided solid guidance to the attending nephrologist on how to treat the patient. Of the 196 kidney biopsies done between 2000 and 2008 for which complete data were available, we determined that 172 (88%) were useful as defined above. In particular, of the 113 kidney biopsies that were done for diagnostic purposes (types 1, 2, 3) 85% were helpful, and all of the procedures done to assess severity were also deemed helpful. From a clinical perspective, categories 1–4 were all considered useful and could have been combined into one group. We divided them into four distinct subcategories to better characterize how nephrologists utilize the information content of a kidney biopsy in a productive manner.
In most circumstances, a renal biopsy is a semi-elective procedure, and technical failures can occur when the procedure fails to obtain adequate tissue. Of all the biopsies analyzed in this study, only 3 were technical failures. The fact that renal biopsies were not useful in 12.2% of cases needs to be considered in assessing the benefit of performing biopsies. In those cases, further testing is needed after the biopsy, and treatment has to be guided by clinical factors rather than the histopathological findings. In our study, we found the overall yield of uninformative biopsies was 12.2%, which is below the 20% threshold that we defined as an acceptable rate. This constitutes an acceptable risk/benefit ratio. Despite the potential risks involved, families can be reassured that a renal biopsy will be helpful in the great majority of patients who must undergo the procedure.
In judging this study, it is worth noting that there has been general uniformity in practice and staffing over the study period. One physician (HT) has been one of the primary nephrologists over the past 20 years and active throughout the 8-year study period and one pathologist (EV) interpreted all the biopsies from 2000 to 2007. It is reasonable to conclude that there was consistency in the use of kidney biopsies to predict, diagnose, and treat patients suspected of having kidney disease. The number of biopsies performed per year (Figure 1) showed no consistent trend, upward or downward, reinforcing the uniformity of the practice. We chose to focus on the years 2000–2008 in order to shed light on the utility of the kidney biopsy during a period that reflects current medical practice. Although it would have been optimal to have the interpretation of all biopsy reports reviewed by the independent observer, the four primary authors agreed in over 80% of cases. Moreover, the physician who performed the kidney biopsy was never involved in the retrospective assessment of diagnostic utility of the procedure. Despite the focused duration of the study and the single center nature of the review, a sufficient number of patients were identified that enabled conclusions to be drawn from our experience.
It is important to acknowledge that the study cannot definitively assess the utility of kidney biopsies performed to determine severity (type 4) in SLE patients. We assumed the results to be useful, excluding those in which a technical failure occurred, because the biopsies identified the WHO class of the disease in all cases and presumably guided treatment by the rheumatologists. This reflects the approach to patient management at Schneider Children’s Hospital in which the care of children with SLE nephritis is delivered primarily by the rheumatologists unless the patients have specific issues such as hypertension, edema, or progress to end stage kidney disease. The utility of the biopsy may vary in those centers where nephrologists directly supervise the full care of patients with SLE. In addition, this study was limited to native kidney biopsies and did not address the value of transplant biopsies. Finally, we have not commented on complications of the procedure because we have reviewed our experience in a previous publication which confirms the overall safety of kidney biopsies performed using ultrasound localization [14].
Based upon clinical experience and perennial difficulties distinguishing between FSGS and MCNS clinically, we anticipated that kidney biopsies performed on these patients would have the highest non-diagnostic rate. Table 2 indicates, however, that the rate of unhelpful biopsies performed on FSGS and MCNS patients was not significantly different compared to biopsies performed for other conditions, and the maximum non-diagnostic rates for any of the major diseases was 10–20%. The entities with higher failure rates involved small numbers of patients, which precludes meaningful conclusions.
It is likely that nephrologists will always have to grapple with the fact that there will be a percentage of biopsies that fail to yield a diagnosis. Too small a percentage suggests too stringent requirements for performing a kidney biopsy. Conversely, a high percentage suggests that kidney biopsies are being performed for inadequate indications. The issue of an acceptable value will vary depending upon the urgency of the patient’s clinical situation, the spectrum of clinical outcomes that might occur, and the availability of treatments that can materially alter the outcome of an anticipated disease entity. For example, pediatric surgeons recognize that not every child with abdominal pain who undergoes a laparotomy should have appendicitis because they realize it is better to occasionally find a normal abdomen rather than manage a ruptured appendix. Interestingly, a recent report in the surgical literature suggests that an acceptable negative appendectomy rate is 10–20%, in the range of our rate of negative kidney biopsies [15]. In view of the spectrum of kidney problems that mandated a biopsy, it may be difficult to define a single acceptable rate of non-diagnostic biopsies, and we offer our findings as a basis for future considerations on this issue.
In summary, we present our findings about the diagnostic value of a kidney biopsy in a varied group of pediatric patients. The overall rate of 12% seems to strike an appropriate balance between maximizing the application and minimizing the risk of this invasive procedure. Our findings may need to be reassessed as clinical information regarding specific disease changes and technical innovations are introduced in the performance of kidney biopsies and handling renal tissue specimens.
Abbreviations
- AIN:
-
Acute interstitial nephritis
- FSGS:
-
Focal segmental glomerulosclerosis
- GFRe:
-
Estimated glomerular filtration rate
- HSP:
-
Henoch-Schonlein purpura
- MCNS:
-
Minimal change nephrotic syndrome
- MPGN:
-
Membranoproliferative glomerulonephritis
- SLE:
-
Systemic lupus erythematosus
- UP/C
: -
Urine protein:creatinine ratio
- WHO:
-
World Health Organization
References
-
Grande JP, Balow JE: Renal biopsy in lupus nephritis. Lupus. 1998, 7: 611-617. 10.1191/096120398678920730.
Article
CAS
PubMedGoogle Scholar
-
Gimenez LF, Micali S, Chen RN, Moore RG, Kavoussi LR, Scheel PJ: Laparoscopic renal biopsy. Kidney Int. 1998, 54: 525-529. 10.1046/j.1523-1755.1998.00006.x.
Article
CAS
PubMedGoogle Scholar
-
Iseki K, Miyasato F, Uehara H, et al: Outcome study of renal biopsy patients in Okinawa, Japan. Kidney Int. 2004, 66: 914-919. 10.1111/j.1523-1755.2004.00836.x.
Article
PubMedGoogle Scholar
-
Kassirer JP: Is renal biopsy necessary for optimal management of the idiopathic nephrotic syndrome?. Kidney Int. 1983, 24: 561-575. 10.1038/ki.1983.194.
Article
CAS
PubMedGoogle Scholar
-
Richter F, Kasabian NG, Irwin RJ, Watson RA, Lang EK: Accuracy of diagnosis by guided renal biopsy of renal mass lesions classified indeterminate by imaging studies. Urology. 2000, 55: 348-352. 10.1016/S0090-4295(99)00468-9.
Article
CAS
PubMedGoogle Scholar
-
Silva DM, Garcia JP, Ribeiro AR, et al: Utility of biopsy in kidney transplants with delayed graft function and acute dysfunction. Transplant Proc. 2007, 39: 376-377. 10.1016/j.transproceed.2007.01.008.
Article
CAS
PubMedGoogle Scholar
-
Stratta R, Canavese C, Marengo M, et al: Risk management of renal biopsy: 1387 cases over 30 years in a single centre. Eur J Clin Invest. 2007, 37: 954-963. 10.1111/j.1365-2362.2007.01885.x.
Article
CAS
PubMedGoogle Scholar
-
Trachtman H, Weiss RA, Bennett B, Greifer I: Isolated hematuria in children: Indications for a renal biopsy. Kidney Int. 1984, 25: 94-99. 10.1038/ki.1984.13.
Article
CAS
PubMedGoogle Scholar
-
Lee YM, Baek SY, Kim JIH, Kim DS, Lee JS, Kim PK: Analysis of renal biopsies performed in children with abnormal findings in urinary mass screenings. Acta Paediatrica. 2006, 95: 849-853. 10.1080/08035250600652005.
Article
PubMedGoogle Scholar
-
Madani A, Fahimi D, Esfehani ST, et al: Glomerular disease in Iranian children: clinico-pathologicalcorrelations. Pediatr Nephrol. 2003, 18: 925-928. 10.1007/s00467-003-1166-5.
Article
PubMedGoogle Scholar
-
Piqueras AI, White RHR, Raafat F, Moghal N, Milford DV: Renal biopsy disease in children presenting with haematuria. Pediatr Nephrol. 1998, 12: 386-391. 10.1007/s004670050471.
Article
CAS
PubMedGoogle Scholar
-
Report of the Southwest Pediatric Nephrology Study Group: A clinico-pathologic study of crescentic glomerulonephritis in 50 children. A report of the Southwest Pediatric Nephrology Study Group. Kidney Int. 1985, 27: 450-458. 10.1038/ki.1985.30.
Article
Google Scholar
-
Schacter AD: Computational simulation of renal biopsy accuracy in focal segmental glomerulosclerosis. Pediatr Nephrol. 2006, 21: 953-957. 10.1007/s00467-006-0127-1.
Article
Google Scholar
-
Gauthier BG, Mahadeo RS, Trachtman H: Techniques for percutaneous renal biopsies. Pediatr Nephrol. 1993, 7: 457-463. 10.1007/BF00857575.
Article
CAS
PubMedGoogle Scholar
-
Colson M, Skinner KA, Dunnington G: High negative appendectomy rates are no longer acceptable. Am J Surg. 1997, 174: 723-726. 10.1016/S0002-9610(97)00183-9.
Article
CAS
PubMedGoogle Scholar
Pre-publication history
-
The pre-publication history for this paper can be accessed here:http://www.biomedcentral.com/1471-2369/10/11/prepub
Download references
Acknowledgements
The authors thank Bernard Gauthier MD for his thoughtful review of the manuscript. In addition, they thank LaTasha Coleman for her assistance in retrieving the patient charts.
Author information
Authors and Affiliations
-
Department of Pediatrics, Division of Nephrology, Schneider Children’s Hospital, New Hyde Park, New York of North Shore-LIJ Health System, Long Island Campus of the Albert Einstein College of Medicine, New York, USA
Bari Scheckner, Alexandra Peyser, Jacob Rube, Freya Tarapore, Rachel Frank, Suzanne Vento, Cathy Hoffman, Beatrice Goilav & Howard Trachtman
-
Department of Pathology, Schneider Children’s Hospital, New Hyde Park, New York of North Shore-LIJ Health System, Long Island Campus of the Albert Einstein College of Medicine, New York, USA
Elsa Valderrama & Douglas Charney
Authors
- Bari Scheckner
You can also search for this author in
PubMed Google Scholar - Alexandra Peyser
You can also search for this author in
PubMed Google Scholar - Jacob Rube
You can also search for this author in
PubMed Google Scholar - Freya Tarapore
You can also search for this author in
PubMed Google Scholar - Rachel Frank
You can also search for this author in
PubMed Google Scholar - Suzanne Vento
You can also search for this author in
PubMed Google Scholar - Cathy Hoffman
You can also search for this author in
PubMed Google Scholar - Elsa Valderrama
You can also search for this author in
PubMed Google Scholar - Douglas Charney
You can also search for this author in
PubMed Google Scholar - Beatrice Goilav
You can also search for this author in
PubMed Google Scholar - Howard Trachtman
You can also search for this author in
PubMed Google Scholar
Corresponding author
Correspondence to
Howard Trachtman.
Additional information
Competing interests
The authors declare that they have no competing interests.
Authors’ contributions
BS, AP, JR and FT retrieved patient data, collated the information and performed data analyses. RF, SV, CH, and BG assisted in patient identification, reviewed biopsy reports. EV and DC performed review of pathology data. BS, AP, and HT wrote the manuscript. HT conceived of the study and designed the retrospective review. All authors read and approved the final version of the manuscript
Authors’ original submitted files for images
Rights and permissions
Open Access
This article is published under license to BioMed Central Ltd. This is an Open Access article is distributed under the terms of the Creative Commons Attribution License (
https://creativecommons.org/licenses/by/2.0
), which permits unrestricted use, distribution, and reproduction in any medium, provided the original work is properly cited.
Reprints and Permissions
About this article
Cite this article
Scheckner, B., Peyser, A., Rube, J. et al. Diagnostic yield of renal biopsies: a retrospective single center review.
BMC Nephrol 10, 11 (2009). https://doi.org/10.1186/1471-2369-10-11
Download citation
-
Received: 01 December 2008
-
Accepted: 21 May 2009
-
Published: 21 May 2009
-
DOI: https://doi.org/10.1186/1471-2369-10-11
Keywords
- Renal Biopsy
- Kidney Biopsy
- Technical Failure
- Negative Appendectomy
- Negative Appendectomy Rate
- Research article
- Open Access
- Published: 21 May 2009
- Alexandra Peyser1,
- Jacob Rube1,
- Freya Tarapore1,
- Rachel Frank1,
- Suzanne Vento1,
- Cathy Hoffman1,
- Elsa Valderrama2,
- Douglas Charney2,
- Beatrice Goilav1 &
- …
- Howard Trachtman1
BMC Nephrology
volume 10, Article number: 11 (2009)
Cite this article
-
8143 Accesses
-
15 Citations
-
Metrics details
Abstract
Background
Previous studies have examined the spectrum of diseases identified with a kidney biopsy and the complications of the procedure. However, few studies have examined the utility of the test to clarify the diagnosis and guide treatment of pediatric patients. This retrospective, single-center chart review was performed to test the hypothesis that at least 80% of native kidney biopsies provide clinically valuable information that rationally guides diagnosis and patient management.
Methods
200 biopsies performed between January 1, 2000 and June 30, 2008 were reviewed. A scheme composed of six categories was devised to classify the utility of each kidney biopsy.
Results
196 complete case files were available for review. Twenty-four (12.2%) biopsies did not shed light on the diagnosis and were unhelpful in patient management – 21 biopsies (10.7%) were non-diagnostic and 3 (1.5%) failed to yield enough tissue for examination. The number of unhelpful biopsies did not cluster in any specific disease entity.
Conclusion
Our findings provide guidance to nephrologists about the total risk of a kidney biopsy, including uninformative results, when seeking informed consent for the procedure. The results suggest an appropriate balance has been reached which maximizes the use of kidney biopsies while minimizing the risk of this invasive procedure (word count: 202).
Peer Review reports
Background
A kidney biopsy is an important diagnostic procedure in nephrology and can aid in determining the appropriate diagnosis, treatment, and prognosis for specific patients. Based upon physical examination, urinalysis and blood tests, physicians attempt to make a clinical diagnosis which is used to guide treatment. This is not always feasible using non-invasive tools, and in such cases a kidney biopsy may need to be performed to confirm or determine the diagnosis, severity, and urgency of therapy.
A kidney biopsy may not always provide information that is needed or pertinent to the clinical scenario. Sometimes an adequate tissue sample of the kidneys cannot be obtained or the information provided from the biopsy fails to shed any light on the patients’ symptoms or clinical data. Due to the invasiveness of the procedure, it is important, when recommending a biopsy for an individual patient, to bear in mind not only the risks of the procedure itself but the distinct possibility that it might prove unhelpful in the patient’s management.
There are a number of recent studies that have detailed the array of diagnoses obtained from kidney biopsies in adults [1–8] and children [9–13] with renal disease. Other reports have assessed the clinical impact that a biopsy may have, but they focused primarily on the risk factors and resulting complications of performing renal biopsies [4]. In this study, we defined a novel system that enabled us to ascertain the usefulness of a particular biopsy by analyzing predictions of the diagnosis pre-biopsy and the physician’s treatment decision post biopsy. Using this scheme, we tested the hypothesis that at least 80% of native kidney biopsies provided clinically valuable information that rationally guided the formulation of the patient’s prognosis and treatment.
Methods
Patients
A database of biopsy procedures was obtained from the Department of Pathology that contained information on all native kidney biopsies completed at Schneider Children’s Hospital between January 1, 2000 and June 31, 2008. The database included the patient’s name, date of biopsy, date of birth, and final diagnosis.
The medical records of patients were retrieved from active clinical files or from off-site storage. The following data were extracted from each available chart: age, gender, blood pressure, dipstick urinalysis results, height (cm), serum creatinine, estimated glomerular filtration rate (GFRe), and urine protein/creatinine ratio in an early morning specimen at the last evaluation prior to the biopsy. In addition, the reason for biopsy, physician’s predicted diagnosis, the biopsy-confirmed diagnosis, and treatment outcome were recorded. The predicted diagnosis was based on the correspondence from the nephrologist who performed the biopsy to the patient’s primary physician or was based on the clinical diagnosis recorded on the biopsy report at the time of submission of the tissue sample.
Classification of diagnostic outcomes of the biopsy: A six-point scheme was designed to determine whether the biopsy served as a useful tool in establishing treatment. If the physician conclusively predicted a particular diagnosis which the biopsy confirmed, the patient was categorized as type 1. A type 2 categorization denoted a biopsy that confirmed one of multiple possible diagnoses. A type 3 categorization accounted for an incorrect pre-biopsy prediction but in which the biopsy finding was conclusive and sufficient to determine appropriate treatment. If the biopsy was used to determine the severity of an established disease, category 4 was assigned to that patient. Failures were identified as either content based or technical and were separated accordingly. Thus, patients in whom the biopsy was insufficient on its own to define prognosis and treatment were categorized as type 5. Technical failures, namely an inability to obtain tissue, were categorized as type 6.
Each case was independently reviewed by one of the four primary authors (AP, JR, BS, FT). Clinical and biopsy reports were recorded and categorized according to the scheme outlined above. Agreement between all pairs of primary reviewers was reached in over 85% of all cases. When there was a discrepancy between the primary reviewers, an independent observer (RF), who did not perform the biopsy, reviewed the case. This reviewer also checked randomly selected charts for accuracy and agreed with the primary reviewers in all cases. A nurse was chosen to adjudicate conflicts among the primary reviewers and to confirm accuracy of the chart reviews because this person would be less likely to be biased in interpreting the utility of the kidney biopsy procedures. The nephrologist who did the kidney biopsy did not participate in the categorization of the informational outcome of the procedure to avoid potential bias.
Statistical Methods
Data are reported as mean ± SD. Differences in proportion were assessed by the chi square or Fisher exact test as appropriate. Differences were considered statistically significant if the P value was <0.05. All information was gathered on a pre-approved form.
Data were de-identified and coded by study number in accordance with the Health Insurance Portability and Accountability Act guidelines (HIPAA). This chart review was approved by the Institutional Review Board of North Shore-LIJ Health System.
Results
A total of 200 biopsies were identified in the pathology database. All charts were retrieved. 4 charts were excluded because the biopsy was done at a different center and the diagnostic assessment and its impact on management by the attending physician could not be directly assessed. Thus, this report is based on the outcomes of 196 kidney biopsies.
The number of biopsies per year is illustrated in Figure 1 which demonstrates a fairly steady rate of performance of this procedure. The vast majority, 183 out of 196 (93%), of the procedures were performed in the outpatient setting. The hospitalized patients represented the cohort in which a kidney biopsy was done to assess acute renal dysfunction. The clinical characteristics of the patients are summarized in Table 1. Of note, 77 (59%) of the patients had UP/C >1 and 30 (15%) had GFRe <90 mL/min/1.73 m2.

This graph illustrates the annual number of biopsies during the study period, 01/2000 – 06/2008.
Full size image
Full size table
Eleven of the patients who had biopsies underwent repeat biopsies. Nine patients had a second biopsy, one had three, and another underwent four procedures. In the last case, of the four biopsies performed, one of the biopsies was a technical failure. In two of these patients, the first biopsies were normal or non-diagnostic and subsequent biopsies showed FSGS and MPGN, respectively. In two other patients, neither the original nor follow up biopsies resulted in a definitive diagnosis. In the remaining 6 patients, the repeat kidney biopsy was done to assess response to treatment, 4 in patients with SLE and 2 in patients with MPGN.
Fifty-eight (29%) patients were classified as type 1, 28 (15%) were type 2, 27 (14%) were type 3, 59 (30%) were type 4 (Figure 2). Of the unsuccessful biopsies, 21 (10.7%) of the biopsies were inconclusive and further testing was required to confirm a diagnosis (type 5). In 3 of these cases, treatment was based upon the clinical findings rather than the histopathological diagnosis reported after the biopsy. In the remaining 18 cases, 5 patients were started on non-immunosuppressive, renoprotective treatment, 8 were followed without initiation of any disease-specific therapy, and 5 were lost to follow-up or transferred to internal medicine nephrology services for further care. Therefore, these biopsies were considered unhelpful. Finally, 3 (1.5%) biopsies failed to yield adequate tissue samples (type 6).

Category 1: Predicted diagnosis confirmed
Category 2: One of several predicted diagnoses confirmed
Category 3: Unexpected but treatable diagnosis made
Category 4: Assessment of disease severity Category 5: Non-diagnostic
Category 6: Technical failure
This graph illustrates the diagnostic categories for the 196 biopsies with complete information that were reviewed. Note that the values for percentage in the pie chart have been rounded off to whole numbers. 1, a biopsy that revealed the specific diagnosis predicted by the physician; 2, a biopsy that confirmed one of multiple possible diagnoses; 3, a biopsy that revealed disease that was different than the pre-biopsy prediction but which was conclusive and sufficient to determine appropriate treatment; 4, a biopsy done to determine the severity of an established disease; 5, a biopsy that was insufficient on its own to define prognosis and treatment; 6, a biopsy that was a technical failure with inability to obtain tissue.
Full size image
The diagnostic utility of the kidney biopsies based on the pre-biopsy diagnosis is summarized in Table 2. The percentage of diagnostically failed biopsies ranged from 0 to 33%. However, focusing on diagnostic entities that contained ≥ 10 patients, there were no significant differences in the rate of this problem for any specific clinical entity.
Full size table
Discussion
In this review, useful biopsies were defined as those that definitively established the diagnosis and which provided solid guidance to the attending nephrologist on how to treat the patient. Of the 196 kidney biopsies done between 2000 and 2008 for which complete data were available, we determined that 172 (88%) were useful as defined above. In particular, of the 113 kidney biopsies that were done for diagnostic purposes (types 1, 2, 3) 85% were helpful, and all of the procedures done to assess severity were also deemed helpful. From a clinical perspective, categories 1–4 were all considered useful and could have been combined into one group. We divided them into four distinct subcategories to better characterize how nephrologists utilize the information content of a kidney biopsy in a productive manner.
In most circumstances, a renal biopsy is a semi-elective procedure, and technical failures can occur when the procedure fails to obtain adequate tissue. Of all the biopsies analyzed in this study, only 3 were technical failures. The fact that renal biopsies were not useful in 12.2% of cases needs to be considered in assessing the benefit of performing biopsies. In those cases, further testing is needed after the biopsy, and treatment has to be guided by clinical factors rather than the histopathological findings. In our study, we found the overall yield of uninformative biopsies was 12.2%, which is below the 20% threshold that we defined as an acceptable rate. This constitutes an acceptable risk/benefit ratio. Despite the potential risks involved, families can be reassured that a renal biopsy will be helpful in the great majority of patients who must undergo the procedure.
In judging this study, it is worth noting that there has been general uniformity in practice and staffing over the study period. One physician (HT) has been one of the primary nephrologists over the past 20 years and active throughout the 8-year study period and one pathologist (EV) interpreted all the biopsies from 2000 to 2007. It is reasonable to conclude that there was consistency in the use of kidney biopsies to predict, diagnose, and treat patients suspected of having kidney disease. The number of biopsies performed per year (Figure 1) showed no consistent trend, upward or downward, reinforcing the uniformity of the practice. We chose to focus on the years 2000–2008 in order to shed light on the utility of the kidney biopsy during a period that reflects current medical practice. Although it would have been optimal to have the interpretation of all biopsy reports reviewed by the independent observer, the four primary authors agreed in over 80% of cases. Moreover, the physician who performed the kidney biopsy was never involved in the retrospective assessment of diagnostic utility of the procedure. Despite the focused duration of the study and the single center nature of the review, a sufficient number of patients were identified that enabled conclusions to be drawn from our experience.
It is important to acknowledge that the study cannot definitively assess the utility of kidney biopsies performed to determine severity (type 4) in SLE patients. We assumed the results to be useful, excluding those in which a technical failure occurred, because the biopsies identified the WHO class of the disease in all cases and presumably guided treatment by the rheumatologists. This reflects the approach to patient management at Schneider Children’s Hospital in which the care of children with SLE nephritis is delivered primarily by the rheumatologists unless the patients have specific issues such as hypertension, edema, or progress to end stage kidney disease. The utility of the biopsy may vary in those centers where nephrologists directly supervise the full care of patients with SLE. In addition, this study was limited to native kidney biopsies and did not address the value of transplant biopsies. Finally, we have not commented on complications of the procedure because we have reviewed our experience in a previous publication which confirms the overall safety of kidney biopsies performed using ultrasound localization [14].
Based upon clinical experience and perennial difficulties distinguishing between FSGS and MCNS clinically, we anticipated that kidney biopsies performed on these patients would have the highest non-diagnostic rate. Table 2 indicates, however, that the rate of unhelpful biopsies performed on FSGS and MCNS patients was not significantly different compared to biopsies performed for other conditions, and the maximum non-diagnostic rates for any of the major diseases was 10–20%. The entities with higher failure rates involved small numbers of patients, which precludes meaningful conclusions.
It is likely that nephrologists will always have to grapple with the fact that there will be a percentage of biopsies that fail to yield a diagnosis. Too small a percentage suggests too stringent requirements for performing a kidney biopsy. Conversely, a high percentage suggests that kidney biopsies are being performed for inadequate indications. The issue of an acceptable value will vary depending upon the urgency of the patient’s clinical situation, the spectrum of clinical outcomes that might occur, and the availability of treatments that can materially alter the outcome of an anticipated disease entity. For example, pediatric surgeons recognize that not every child with abdominal pain who undergoes a laparotomy should have appendicitis because they realize it is better to occasionally find a normal abdomen rather than manage a ruptured appendix. Interestingly, a recent report in the surgical literature suggests that an acceptable negative appendectomy rate is 10–20%, in the range of our rate of negative kidney biopsies [15]. In view of the spectrum of kidney problems that mandated a biopsy, it may be difficult to define a single acceptable rate of non-diagnostic biopsies, and we offer our findings as a basis for future considerations on this issue.
In summary, we present our findings about the diagnostic value of a kidney biopsy in a varied group of pediatric patients. The overall rate of 12% seems to strike an appropriate balance between maximizing the application and minimizing the risk of this invasive procedure. Our findings may need to be reassessed as clinical information regarding specific disease changes and technical innovations are introduced in the performance of kidney biopsies and handling renal tissue specimens.
Abbreviations
- AIN:
-
Acute interstitial nephritis
- FSGS:
-
Focal segmental glomerulosclerosis
- GFRe:
-
Estimated glomerular filtration rate
- HSP:
-
Henoch-Schonlein purpura
- MCNS:
-
Minimal change nephrotic syndrome
- MPGN:
-
Membranoproliferative glomerulonephritis
- SLE:
-
Systemic lupus erythematosus
- UP/C
: -
Urine protein:creatinine ratio
- WHO:
-
World Health Organization
References
-
Grande JP, Balow JE: Renal biopsy in lupus nephritis. Lupus. 1998, 7: 611-617. 10.1191/096120398678920730.
Article
CAS
PubMedGoogle Scholar
-
Gimenez LF, Micali S, Chen RN, Moore RG, Kavoussi LR, Scheel PJ: Laparoscopic renal biopsy. Kidney Int. 1998, 54: 525-529. 10.1046/j.1523-1755.1998.00006.x.
Article
CAS
PubMedGoogle Scholar
-
Iseki K, Miyasato F, Uehara H, et al: Outcome study of renal biopsy patients in Okinawa, Japan. Kidney Int. 2004, 66: 914-919. 10.1111/j.1523-1755.2004.00836.x.
Article
PubMedGoogle Scholar
-
Kassirer JP: Is renal biopsy necessary for optimal management of the idiopathic nephrotic syndrome?. Kidney Int. 1983, 24: 561-575. 10.1038/ki.1983.194.
Article
CAS
PubMedGoogle Scholar
-
Richter F, Kasabian NG, Irwin RJ, Watson RA, Lang EK: Accuracy of diagnosis by guided renal biopsy of renal mass lesions classified indeterminate by imaging studies. Urology. 2000, 55: 348-352. 10.1016/S0090-4295(99)00468-9.
Article
CAS
PubMedGoogle Scholar
-
Silva DM, Garcia JP, Ribeiro AR, et al: Utility of biopsy in kidney transplants with delayed graft function and acute dysfunction. Transplant Proc. 2007, 39: 376-377. 10.1016/j.transproceed.2007.01.008.
Article
CAS
PubMedGoogle Scholar
-
Stratta R, Canavese C, Marengo M, et al: Risk management of renal biopsy: 1387 cases over 30 years in a single centre. Eur J Clin Invest. 2007, 37: 954-963. 10.1111/j.1365-2362.2007.01885.x.
Article
CAS
PubMedGoogle Scholar
-
Trachtman H, Weiss RA, Bennett B, Greifer I: Isolated hematuria in children: Indications for a renal biopsy. Kidney Int. 1984, 25: 94-99. 10.1038/ki.1984.13.
Article
CAS
PubMedGoogle Scholar
-
Lee YM, Baek SY, Kim JIH, Kim DS, Lee JS, Kim PK: Analysis of renal biopsies performed in children with abnormal findings in urinary mass screenings. Acta Paediatrica. 2006, 95: 849-853. 10.1080/08035250600652005.
Article
PubMedGoogle Scholar
-
Madani A, Fahimi D, Esfehani ST, et al: Glomerular disease in Iranian children: clinico-pathologicalcorrelations. Pediatr Nephrol. 2003, 18: 925-928. 10.1007/s00467-003-1166-5.
Article
PubMedGoogle Scholar
-
Piqueras AI, White RHR, Raafat F, Moghal N, Milford DV: Renal biopsy disease in children presenting with haematuria. Pediatr Nephrol. 1998, 12: 386-391. 10.1007/s004670050471.
Article
CAS
PubMedGoogle Scholar
-
Report of the Southwest Pediatric Nephrology Study Group: A clinico-pathologic study of crescentic glomerulonephritis in 50 children. A report of the Southwest Pediatric Nephrology Study Group. Kidney Int. 1985, 27: 450-458. 10.1038/ki.1985.30.
Article
Google Scholar
-
Schacter AD: Computational simulation of renal biopsy accuracy in focal segmental glomerulosclerosis. Pediatr Nephrol. 2006, 21: 953-957. 10.1007/s00467-006-0127-1.
Article
Google Scholar
-
Gauthier BG, Mahadeo RS, Trachtman H: Techniques for percutaneous renal biopsies. Pediatr Nephrol. 1993, 7: 457-463. 10.1007/BF00857575.
Article
CAS
PubMedGoogle Scholar
-
Colson M, Skinner KA, Dunnington G: High negative appendectomy rates are no longer acceptable. Am J Surg. 1997, 174: 723-726. 10.1016/S0002-9610(97)00183-9.
Article
CAS
PubMedGoogle Scholar
Pre-publication history
-
The pre-publication history for this paper can be accessed here:http://www.biomedcentral.com/1471-2369/10/11/prepub
Download references
Acknowledgements
The authors thank Bernard Gauthier MD for his thoughtful review of the manuscript. In addition, they thank LaTasha Coleman for her assistance in retrieving the patient charts.
Author information
Authors and Affiliations
-
Department of Pediatrics, Division of Nephrology, Schneider Children’s Hospital, New Hyde Park, New York of North Shore-LIJ Health System, Long Island Campus of the Albert Einstein College of Medicine, New York, USA
Bari Scheckner, Alexandra Peyser, Jacob Rube, Freya Tarapore, Rachel Frank, Suzanne Vento, Cathy Hoffman, Beatrice Goilav & Howard Trachtman
-
Department of Pathology, Schneider Children’s Hospital, New Hyde Park, New York of North Shore-LIJ Health System, Long Island Campus of the Albert Einstein College of Medicine, New York, USA
Elsa Valderrama & Douglas Charney
Authors
- Bari Scheckner
You can also search for this author in
PubMed Google Scholar - Alexandra Peyser
You can also search for this author in
PubMed Google Scholar - Jacob Rube
You can also search for this author in
PubMed Google Scholar - Freya Tarapore
You can also search for this author in
PubMed Google Scholar - Rachel Frank
You can also search for this author in
PubMed Google Scholar - Suzanne Vento
You can also search for this author in
PubMed Google Scholar - Cathy Hoffman
You can also search for this author in
PubMed Google Scholar - Elsa Valderrama
You can also search for this author in
PubMed Google Scholar - Douglas Charney
You can also search for this author in
PubMed Google Scholar - Beatrice Goilav
You can also search for this author in
PubMed Google Scholar - Howard Trachtman
You can also search for this author in
PubMed Google Scholar
Corresponding author
Correspondence to
Howard Trachtman.
Additional information
Competing interests
The authors declare that they have no competing interests.
Authors’ contributions
BS, AP, JR and FT retrieved patient data, collated the information and performed data analyses. RF, SV, CH, and BG assisted in patient identification, reviewed biopsy reports. EV and DC performed review of pathology data. BS, AP, and HT wrote the manuscript. HT conceived of the study and designed the retrospective review. All authors read and approved the final version of the manuscript
Authors’ original submitted files for images
Rights and permissions
Open Access
This article is published under license to BioMed Central Ltd. This is an Open Access article is distributed under the terms of the Creative Commons Attribution License (
https://creativecommons.org/licenses/by/2.0
), which permits unrestricted use, distribution, and reproduction in any medium, provided the original work is properly cited.
Reprints and Permissions
About this article
Cite this article
Scheckner, B., Peyser, A., Rube, J. et al. Diagnostic yield of renal biopsies: a retrospective single center review.
BMC Nephrol 10, 11 (2009). https://doi.org/10.1186/1471-2369-10-11
Download citation
-
Received: 01 December 2008
-
Accepted: 21 May 2009
-
Published: 21 May 2009
-
DOI: https://doi.org/10.1186/1471-2369-10-11
Keywords
- Renal Biopsy
- Kidney Biopsy
- Technical Failure
- Negative Appendectomy
- Negative Appendectomy Rate
Диагностика заболеваний редко обходится без инструментальных и лабораторных исследований. Оценки симптомов недостаточно — нужно узнать, что происходит внутри органов и тканей. Одним из наиболее точных методов обследования является биопсия. Врач производит забор тканевого материала в области предполагаемого патологического процесса с целью его дальнейшего изучения. Микроскопический анализ полученного образца помогает выявить характерные для определенного заболевания изменения. В онкологической практике биопсия считается информативным методом уточнения типа опухоли, ее стадирования.
- Что это за анализ?
- Показания к проведению
- Виды и способы проведения биопсии
- Подготовка
- Может ли биопсия быть ошибочной?
Что это за анализ?
Биопсия — высокоинформативный способ обследования, применяемый в случае необходимости анализа клеток в определенной анатомической области. Забор тканей с их последующим обследованием с помощью микроскопии дает возможность точно оценить клеточный состав. Без такой процедуры сложно обойтись, если врач подозревает наличие доброкачественного или злокачественного новообразования в определенном органе. Это уточняющее исследование, дополняющее результаты других диагностических процедур. Онколог анализирует результаты биопсии, рентгенографии, эндоскопии и иммунологических тестов совместно.
Онкологические заболевания развиваются быстро и угрожают жизни пациента. Нужно как можно раньше выбрать наиболее эффективную схему лечения. Именно с этой целью проводится биопсия. По результатам процедуры врач приходит к выводу, какие травматичные или даже опасные с точки зрения осложнений способы лечения уместны в данном случае. Подбирается тактика оперативного вмешательства, радиотерапии, химиотерапевтического лечения. Все это было бы невозможно без точного определения типа опухоли, ее стадии и распространенности в организме. Нужны цитологические и гистологические тесты.
В качестве примера можно привести злокачественное новообразование прямой кишки, растущее в нижней части органа. В качестве основного метода лечения выполняется иссечение этой анатомической структуры с последующим формированием колостомы для выделения каловых масс. Если диагноз не был полностью подтвержден, подобное вмешательство не проводят. Оно может по ошибке сделать пациента инвалидом.
Показания к проведению
Подобная диагностическая процедура требуется, если врач предполагает о наличии патологического процесса, подтверждение которого невозможно с помощью других способов исследования. В большинстве случаев это онкологические болезни, однако область применения биопсии ими не ограничивается. Например, такое исследование часто назначают гастроэнтерологи для оценки состояния слизистой оболочки органов пищеварительного тракта. Определяется вид воспалительного процесса, подбирается способ его лечения. В гинекологии и эндокринологии этот метод дает возможность определить причину нарушения фертильности, обнаружить ранние признаки воспаления и дисплазии.
Также биопсия необходима для определения особенностей течения и степени тяжести патологического процесса при болезнях печеночной ткани, почек, головного мозга, мышц и других анатомических структур. Это важно для подбора и изменения схемы медикаментозной терапии. По результатам анализа врач определяет прогностические данные.
Виды и способы проведения биопсии
В современной клинической практике чаще всего используют следующие методики выполнения биопсии:
- Мазки, соскобы и бритвенный метод. Зачастую специалисту требуется небольшое количество материала для постановки диагноза. Можно выполнить мазок и получить все необходимые данные при его последующей микроскопии. Например, такой способ часто применяют в гинекологии. Бритвенная биопсия предполагает иссечение тонкого участка кожного покрова с помощью скальпеля или другого инструмента.
- Тонкоигольная пункция. Такая процедура тоже подходит для случаев, когда достаточно получить немного клеток. В область предполагаемого патологического процесса вводится тонкая игла, захватывающая тканевой образец.
- Толстоигольная пункция. Позволяет произвести забор большого образца тканей без иссечения. Ее назначают при злокачественном новообразовании молочной железы, печеночной ткани, предстательной железы. Трепан-биопсия подходит для исследования кожного покрова, костномозговых структур. Используется специальный инструмент в форме цилиндра.
- Аспирационный метод. Это современная техника забора материала, при котором используется вакуумный прибор в форме цилиндра. В качестве механизма применяется отрицательное давление. Прибор присоединяют к игле. Аспирация дает возможность взять несколько образцов в разных участках анатомической структуры.
- Операционная биопсия. Проводится непосредственно во время операции, когда врач иссекает опухолевую ткань. Это высокоинформативное исследование, позволяющее оценить состояние большого количества тканей. Минус такого вида процедуры — определить тип болезни можно только после операции. Плюсом можно считать совмещение лечебной практики с достоверной диагностикой.
- Эндоскопическая биопсия. Проводится во время диагностики внутренних полостных структур, вроде пищеварительного или респираторного тракта. С помощью эндоскопа врач осматривает подозрительные участки тканей и выбирает место забора материала. Плюсом такой техники можно считать повышенную точность результатов исследования.
Способ проведения диагностики выбирают в зависимости от анамнеза пациента.
Подготовка
В большинстве случаев специально готовиться не следует. Достаточно прийти к врачу в день проведения процедуры и подписать необходимые документы. Специалист объяснит, как будет проходить обследование. Расскажет о рисках и возможных неприятных ощущениях. Определенные виды биопсии выполняют под местным обезболиванием. Реже требуется наркоз. Пациент может сам выбирать комфортный для него способ выполнения диагностики. В случае наркоза нужны специальные подготовительные процедуры.
Для биопсии характерны стандартные осложнения, возникающие при других видах вмешательств. Возможно кровоизлияние, инфицирование тканей. Реже возникает травматизация внутренних органов. Такие негативные последствия редки, но врач обязательно уведомляет пациента о рисках.
Может ли биопсия быть ошибочной?
Достоверность исследования зависит от способа его проведения, анамнеза пациента, опыта врача и других факторов. Например, при пункции специалист может получить образец тканей без злокачественных клеток, если игла попала в соседнюю с опухолью область. В этом случае возможен ложноположительный результат. Онкологи учитывают такую вероятность, и всегда назначают уточняющие исследования. Диагноз не ставится только на основе результатов одной процедуры. Всегда проводится комплексная оценка состояния организма.
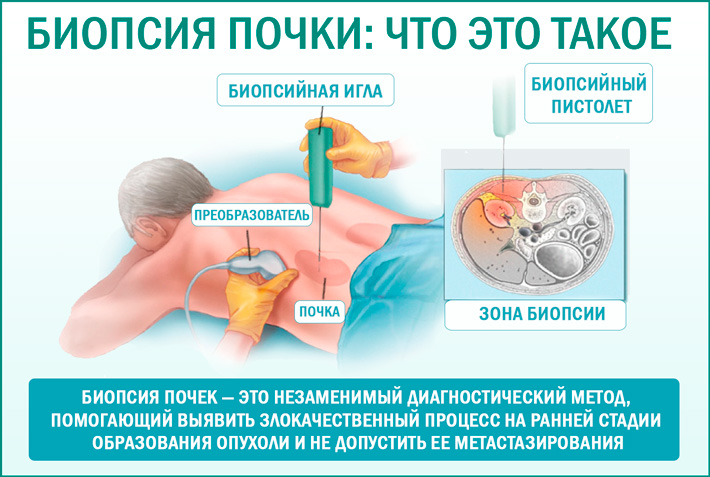
Биопсия почки (почечная биопсия) — это образец, взятый из ткани почки, который обрабатывается специальным образом и затем исследуется под микроскопом в лаборатории.
Как проводится биопсия?
Ключевая мера для безопасной биопсии — обеспечение четкой визуализации почек и места инъекции. Это гарантирует, с одной стороны, получение достаточно большого и четкого образца ткани из почки, с другой, снижает риск повреждения органа.
Для этой цели, например, подходит компьютерная томография. Обследование обычно проводят как до, так и во время процедуры. Кроме томографии могут использоваться различные методы визуализации, но чаще всего уролог выбирает ультразвук — УЗИ почек, рентген (рентген) или их комбинацию. Среди всех методов, КТ будет самым дорогим.
При использовании рентгеновского снимка пациенту в некоторых случаях в вену вводится рентгеноконтрастное средство, что позволяет более точно отображать почки на экране рентгеновского аппарата. Контрастное вещество концентрируется в почках, а затем выделяется с мочой. Необходимость применения контраста определяется урологом, и зависит от патологии и места взятия образцов.
После определения положения почки, место биопсии десенсибилизируется препаратом, который транспортируется вглубь ткани через шприц к почке. Пациент не чувствует боли, хотя процедура несколько неприятная. Важное условие: следует обращать внимание на аллергию на анестетик или контрастное вещество.
Биопсия почек проводится специальной двойной иглой для биопсии, которая вводится через задние мышцы в почку. Врач отбирает 1-2 образца ткани почки длиной около 1-2 см и толщиной около 1,5 мм и отправляет их для дальнейшей обработки в лабораторию. Это обследование часто используется для диагностики заболеваний, которые поражают почечную ткань примерно одинаково в обеих почках. В этом случае достаточно взять образец только из одной почки: результат, полученный от другой почки, будет таким же или похожим.
В конце процедуры место инъекции обрабатывают и накладывают повязку. Вся процедура вместе с подготовкой в зависимости от обстоятельств занимает 30-60 минут.
Первые предварительные выводы БП можно ожидать в течение 1-2 дней, но окончательные результаты биопсии можно получить только через пару недель.
Что необходимо для того, чтобы биопсия почек прошла успешно и без осложнений?
До биопсии врач должен быть проинформирован о любом серьезном заболевании у пациента. К сожалению, уролог не может проверить все противопоказания — это займет несколько недель и обойдется в большую сумму, поэтому обязанность информации об имеющихся патологиях возложена на больного. В частности, важно сообщить о наличии аллергии, хронических заболеваний, инфекций.
Во время процедуры врач предупреждает, когда нужно вдыхать или выдыхать, а когда не дышать. Следует строго соблюдать время задержки дыхания, поскольку в это время врач вводит иглу, и любые движения могут привести к изменениям в положении почек, что увеличить риск возможных травм и объем тканей, затронутых вмешательством. Дыхание задерживается максимум на 10–20 секунд — с этим может справиться подавляющее большинство пациентов.
После биопсии необходим строгий постельный режим до утра. Пациент должен находиться в лежачем положении. Также придется ограничить еду, так как это может вызвать кровотечение из места инъекции или вокруг почки.
В течение первых нескольких часов у пациента на спине остается компрессионная повязка, которую нельзя снимать. Если на спине лежать тяжело, можно ненадолго повернуться на бок или даже на живот, но большую часть времени пациент должен лежать на спине.
После почечной биопсии пациент должен выпить около 1,5 литров жидкости в течение часа и выпить как можно больше воды до конца дня. Это увеличит выработку мочи, которая оказывает давление на почечную ткань изнутри и, таким образом, снижает риск кровотечения.
Если функция почек пациента значительно нарушена, врач сам определит необходимое количество жидкости.
Может ли почечная биопсия дать осложнения?
Это возможно, но очень редко. По статистике осложнения возникают у 1-2 пациентов из 100. Чтобы этого избежать, после биопсии обычно выполняют ультразвуковую проверку почек. Она часто показывает небольшой отток крови в почку или вокруг нее, что не является серьезным осложнением — это обычный побочный эффект — реакция на травму.
- В редких случаях у пациента отток крови может быть более или более болезненным. В итоге может потребоваться сосудистое вмешательство (эмболизация) или хирургическое лечение.
- В редких случаях после биопсии может возникнуть кровотечение в мочевыводящих путях или инфекция в месте инъекции. В этом случае проводится антибиотикотерапия.
Возможность осложнений нельзя недооценивать, но биопсия почки обычно назначается при обстоятельствах, когда возникла необходимость постановки точного диагноза, и выявить заболевание можно только таким методом. Важность результата значительно превышает потенциальный риск осложнений инвазивной хирургии, поэтому отказываться от биопсии не стоит.
Может ли забор тканей нарушить функцию почек?
Количество собираемой ткани настолько мало (около 20 почечных клубочков из миллиона в одной почке), что процедура не может оказать никакого влияния.
Как вести себя после биопсии почек?
Как правило, в течение 2-х недель после биопсии следует соблюдать следующие рекомендации:
- Следует исключить физические нагрузки.
- Необходимо избегать тряски тела (не рекомендуется даже спускаться по лестнице).
- Не рекомендуется принимать горячую ванну, поэтому пациент должен выбирать только душ.
- Нельзя поднимать тяжелые предметы;
- Нужно отказаться от всех видов деятельности, которые могут привести к травме поясничного или брюшного отдела.
Через 2-3 недели после биопсии почек пациент может вернуться к обычному режиму, при условии отсутствия осложнений.
[dcb id=9583]
Почечно-клеточный рак (ПКР) составляет около 2% всех опухолей у взрослых (Parkin, 2005). В США ПКР был диагностирован у 36 000 пациентов (22 000 мужчин и 14 000 женщин) (Jemal, 2005). C 1973 по 1997 гг. количество вновь зарегистрированных случаев ПКР в США возросло на 43%, а смертность увеличилась на 16%. В Европе смертность от ПКР росла до 1990-х гг. С середины 90-х гг. XX века уровень смертности стабилизировался. Наибольшее снижение наблюдалось в Германии, Норвегии и Нидерландах (Levi, 2004). В России рак почки диагностируется примерно у 15000 людей в год. В общей структуре онкологических заболеваний рак почки занимает 3% от всех злокачественных опухолей (Bray F., 2003, Levi F., 2004).
Биопсия является важным методом верификации опухолевого процесса и стратегического определения лечебной тактики. Однако не во всех клиниках с целью определения показаний к оперативному лечению у пациентов с опухолями почек выполняется биопсия.
Это обусловлено несколькими факторами:
- сегодня в урологии имеется много достоверных высокоспецифичных, высокочувствительных, эффективных и доступных методов диагностики: УЗИ, КТ, МРТ;
- специфичность этих методов исследования не зависит от размера опухоли;
- широкое развитие и внедрение в клиническую практику нефронсберегающих методик лечения почечно-клеточного рака, в том числе и лапароскопии;
- возможные осложнения биопсии;
- себестоимость исследования.
Возникает дилемма: мы действительно активно выступаем «за» биопсию, когда это касается опухоли мочевого пузыря или простаты, и почему-то игнорируем биопсию при опухолях почки.
Сегодня наша хирургическая активность очень высока – мы оперируем пациентов с любой стадией по TNM опухоли почки, любой степени сложности (таблица 1).
Таблица 1. Количественное распределение опухолей почек по гистологической структуре
| Распределение новообразований почек по нозологии у прооперированных больных Ставропольского района и г. Тольятти за период с 1997 по 2001 гг. | 1997 | 1998 | 1999 | 2000 | 2001 | Итого |
|---|---|---|---|---|---|---|
| Всего прооперированы | 44 | 42 | 46 | 45 | 72 | 249 |
| Неклассифицируемый рак | 5 | 1 | 3 | 0 | 10 | 19 |
| Папиллярный рак 1-го и 2-го типов | 1 | 1 | 3 | 3 | 3 | 11 |
| Онкоцитома | 0 | 1 | 3 | 3 | 4 | 11 |
| Ангиомиолипома | 0 | 6 | 2 | 2 | 8 | 18 |
| Хромофобный рак | 0 | 1 | 1 | 1 | 1 | 4 |
| Мультилокулярная кистозная нефрома | 0 | 0 | 1 | 1 | 1 | 3 |
| Светлоклеточный рак | 38 | 32 | 33 | 35 | 45 | 183 |
Плешивцев М.А., Саратов, 2007
Следует отметить тот факт, что благодаря высокой чувствитель ности и специфичности лучевых методов диагностики все больше увеличивается процент выявления маленьких опухолей, которые выделены в отдельную стадию Т1а. Лечение маленьких опухолей почки стало второй по важности проблемой после лекарственной резистентности при поздних стадиях заболевания. Для опухолей размером менее 3 см была выявлена тенденция к медленному росту и редкому метастазированию. В связи с этим, бытует мнение о целесообразности проведения биопсии перед хирургическим лечением с целью оценки реальной необходимости хирургического вмешательства в данный конкретный момент. Если опухоль является низкодифференцированной, хирургическая операция имеет смысл именно в данное время. В скором времени, несомненно, появятся новые геномные и другие методы анализа биопсийного материала, которые позволят прогнозировать целесообразность лечения.
В настоящее время лучевые методы диагностики являются основными в обнаружении опухолей почек. Компьютерная томография позволяет верифицировать диагноз практически в 100% случаев, поэтому мы не задумываемся о необходимости биопсии. К сожалению, процент выявления запущенных стадий опухолей почек остается высоким: в стадии Т3 – до 39%, Т4 – до 40% случаев (Kavashima A. et al., 2004).
Неоспорим тот факт, что все лучевые методы диагностики позволяют нам верифицировать диагноз практически в 100% случаев, поэтому мы не задумываемся о необходимости биопсии.
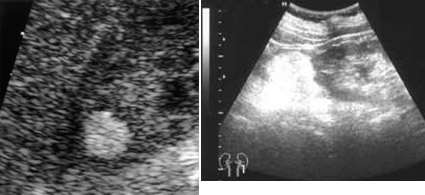
В середине 50-х годов прошлого века впервые появился метод ультразвукового исследования (УЗИ), благодаря ему количество случайно выявленных опухолей почек выросло с 10% в 1970-х гг. до 68% в 1998 г. Если при рутинном УЗИ обнаруживается киста почки, относящаяся к третьему типу по классификации Bosniak, то биопсия должна выполняться обязательно. Однако надо отметить тот факт, что при сочетанном использовании компьютерной томографии (КТ) с УЗ-диагностикой диагноз рака почки возможно достоверно установить и без биопсии.
Ангиомиолипомы – это тоже одна из проблем, наиболее часто встречающихся в амбулаторной практике в виде случайной находки при УЗИ (рисунок 1). Если при ангиомиолипоме выполнять биопсию, чтобы исключить злокачественный компонент опухоли, то можно столкнуться с определенным процентом осложнений. В данном случае сочетание УЗИ и КТ-диагностики также достаточно, чтобы установить диагноз ангиомиолипомы и не подвергать больного биопсии (Nelson C.P., 2002, Oesterling J.E., 1986).
Рисунок1. УЗИ. Ангиомиолипома
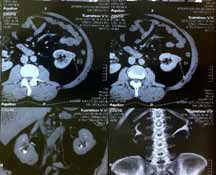
Еще один метод визуализации, применяющийся для диагностики опухолевого процесса – магнитно-резонансная томография (МРТ). Ценность и доступность МРТ в стадировании опухолевого процесса, оценке инвазии фиброзной капсулы почки, поражению лимфоузлов, – неоспорима, но этот диагностический поиск все равно приведет нас к осознанию необходимости операции.
Информативность МРТ и КТ также стремится к 100%, причем это касается любой стадии заболевания (Палко А., 1991) (рисунок 2).
Рисунок 2. КТ в диагностике опухолей почек
Итак, вопрос о биопсии особенно остро стоит для маленьких опухолей почек, определения дальнейшей тактики в отношении пациентов – активное наблюдение или хирургическое лечение? В результате проведенных исследований доказано, что даже при небольших опухолях почек имеется риск метастазирования: не существует безопасных размеров опухоли. При размерах опухоли меньше 2 см, опухоль ассоциированная смертность составляет 4,3%, менее 4 см – 6,2%; а частота метастазирования при таких размерах опухоли – 5,2% (Tsui K.H., 1997). Поэтому, даже, несмотря на маленькие размеры опухоли, невозможно гарантировать пациенту отсутствие метастазирования. Даже опухоли, которые называются доброкачественными, являются условно-доброкачественными.
С деонтологической точки зрения ситуация также неоднозначна. Предложим пациенту с маленькой опухолью почки на выбор две ситуации. Первая – предложить биопсию опухоли и при отсутствии злокачественного процесса рекомендовать динамическое наблюдение. Вторая – предложить сразу выполнить лапароскопическую операцию (например, резекцию почки) или аблятивную методику (криоабляцию)
образования в почке. Если пациента информировать о возможном ложноотрицательном результате биопсии, который, в среднем, встречается в 5% случаев (Peters C., 2005), ее возможных осложнениях, и обусловно доброкачественном характере опухоли, то, скорее всего, он сразу выберет операцию.
Биопсия, как и любая инвазивная процедура, может иметь осложнения, которые или требуют дополнительного вмешательства, или делают биопсию неинформативной (таблица 2). Это такие осложнения, как неадекватный биоптат (до 10%), микро- и макрогематурия (5-9%), бессимптомная паранефральная гематома (до 90% случаев), кровотечения, требующие гемотрансфузии, травма соседних органов (Tang S., 2002, Cluzel P., 2000). В самых серьезных случаях биопсия опухоли почки может закончиться хирургическим вмешательством, вплоть до нефрэктомии.
Таблица 2. Частота и структура осложнений биопсии почек
| Осложнения | Частота (%) |
|---|---|
| Неадекватный биоптат | 2-3-5-10 |
| Микрогематурия | 100 |
| Макрогематурия | 5-9 |
| Бессимптомная перинефральная гематома | 90 |
| Симптоматическая перинефральная гематома | < 20 |
| Кровотечения, требующие гемотрансфузии | < 3 |
| Кровотечения, требующие хирургического вмешательства | < 0,2 |
| Травма прилегающих органов | < 1,0 |
| Инфицирование (при отсутствии пиелонефрита) | < 1,0 |
| Не требующие вмешательства артериовенозные фистулы | 15-18 |
| Требующие вмешательства артериовенозные фистулы | < 1,0 |
| Нефрэктомия | 0,02-0,06 |
| Летальные исходы | < 0,1 |
Так все же где место для биопсии? Нельзя категорически утверждать, что биопсия не нужна при опухолях почек. Однако, благодаря тем методам диагностики, которые сегодня имеются в арсенале урологов, биопсии почки, как дополнительной инвазии, сопряженной с осложнениями, в большинстве случаев опухолей почки можно избежать (таблица 3).
Таблица 3. Осложнения биопсии
| Центр | Количество пациентов с серьезными осложнениями |
Количество биопсий |
Процентная доля серьезных осложнений |
|---|---|---|---|
| 1 | 4 | 54 | 7,4 |
| 2 | 4 | 28 | 14,3 |
| 3 | 0 | 12 | 0 |
| 4 | 3 | 110 | 2,7 |
| 5 | 5 | 25 | 20 |
| 6 | 8 | 71 | 8,8 |
| 7 | 0 | 36 | 0 |
| 8 | 8 | 26 | 30,8 |
| 9 | 10 | 36 | 27,8 |
| 10 | 6 | 24 | 25 |
| 11 | 7 | 89 | 7,9 |
| Всего | 55 | 531 | 10,4 |
F. Hussian, M. Mallik, 2009
Заключение
• Возможно, биопсия опухоли почки нужна пациентам, которым планируются аблятивные методы хирургического лечения: криоабляция, HIFU-терапия, термоабляция, РЧА. Но и в этом случае биопсию экспресс мето-дом можно выполнить в момент проведения операции.
• Пациенты с неопределяемыми лучевыми методами образованиями почек достаточно редки; однако, проводя комплексное обследование таких пациентов, удается поставить диагноз без биопсии.
• Пациентам, отказывающимся от оперативного лечения, возможно, следует рекомендовать выполнить биопсию опухоли. Если по результатам гистологического заключения будут обнаружены злокачественные клетки, то есть шанс, что пациент более благосклонно отнесется к предложенному оперативному лечению.
• Пациенты с метастатической болезнью в крайне тяжелом состоянии и/или неоперабельные больные – это пациенты, которым надо верифицировать диагноз с помощью биопсии и определиться с проведением химиотерапии, таргетной терапии. Хотелось бы поделиться и собственным опытом, полученным на базе НИИ урологии (таблица 4).
Таблица 4. Опыт НИИ урологии
| Операции | 2009 год | 2010 год |
|---|---|---|
| Радикальная нефрэктомия | 48 | 72 |
| Лапароскопическая нефрэктомия | 6 | 25 |
| Нефруретерэктомия | 3 | 11 |
| Резекция почки | 10 | 24 |
| Лапароскопическая резекция почки | — | 2 |
| Всего | 67 | 134 |
| Гистологически – рак | 66 | 133 |
| Ангиомиолипома | 1- 1,49%- 1,56% | 1- 0,75%- 0,8% |
В 2010 г. нами выполнено 72 открытых радикальных нефрэктомии, 25 лапароскопических нефрэктомий, 24 открытых и 2 лапароскопические резекции почек, 11 нефроуретерэктомий, всего – 134 операции. По результатам гистологического заключения из 134 операций в 133 случаях выявлен рак почки. У одного больного диагностирована ангиомиолипома, что составляет 0,8% случаев.
Ключевые слова: рак почки, биопсия почки.
Keywords: kidney cancer, kidney biopsy
| Прикрепленный файл | Размер |
|---|---|
| Скачать статью | 713.23 кб |
ГКБ№ 52 – ведущий нефрологический центр страны, при котором функционирует сектор морфологической диагностики почечной патологии. В год здесь исследуется около 1,5 тыс. материалов биопсии. Руководит центром Екатерина Сергеевна Столяревич, доктор медицинских наук, профессор, эксперт с мировым именем в области морфологической диагностики заболеваний почек. Почечные биоптаты для исследования сюда привозят из всех больниц столицы и более чем 50 стационаров России.
Назначают и проводят биопсию почки врачи-нефрологи. О том, зачем и в каких случаях нужна биопсия, как проводится процедура, как сделать исследование в 52-й больнице, рассказывает Екатерина Сергеевна Иванова, кандидат медицинских наук, врач-нефролог отделения патологии трансплантированной почки ГКБ №52
Зачем и кому нужна биопсия?
Биопсия нужна для верификации диагноза. Нефрологических заболеваний множество, подходы к лечению, главная цель которого избежать или максимально отсрочить развитие почечной недостаточности, в каждом случае разные. Чем точнее диагноз, тем эффективнее лечение. Во многих случаях мы назначаем патогенетическую терапию, то есть лечение, которое воздействует на механизмы развития заболевания. Используем «серьезные» препараты, например, иммуносупрессоры и гормоны. Действовать вслепую здесь никак нельзя.
Показания для проведения биопсии — наличие белка в суточном анализе мочи в количестве больше одного грамма и/или повышенный уровень креатинина в крови, который указывает на нарушение функции работы почек.
Однако биопсия требуется далеко не всегда. Если говорить о пациентах стационара, то есть людей с тяжелыми заболеваниями почек, в биопсии нуждается примерно половина. Среди тех, кто наблюдается амбулаторно у нефролога — гораздо меньше.
Международные клинические рекомендации описывают случаи, когда биопсию можно не делать. Некоторые диагнозы мы можем точно поставить на основании лабораторных исследований. Например, окончательно подтвердить мембранозную нефропатию можно с помощью анализа крови, на нее укажут определенные показатели. И можно сразу начинать лечение.
Бывает и так, что биопсию делать уже поздно, потому что мы не получим полезной информации. Если УЗИ — ультразвуковое исследование почек, которое обязательно проводится перед биопсией, показывает, что почки сморщены и значительно уменьшились в размерах, значит, почечная ткань уже заместилась рубцовой тканью. Восстановить функцию органа в этом случае вряд ли возможно, а пациента надо готовить к заместительной почечной терапии – к диализу.
Напомню, что почки- «молчаливый орган», заболевания могут никак не проявляться длительное время, или могут быть отнесены на счет других недомоганий. В описанной ситуации могут оказаться люди, даже не подозревающие, что у них есть проблемы с почками. Но ведь ее можно было бы избежать. Чтобы вовремя увидеть изменения – достаточно общего анализа мочи с оценкой уровня белка и мочевого осадка и биохимического анализа крови (креатинин и мочевина), которые можно сделать как в рамках диспансеризации, так и самостоятельно. Уремическая интоксикация (когда почки не справляются с выведением токсинов из организма), проявляющаяся в виде отеков, тошноты, отсутствия аппетита и потери веса, неприятного запаха из рта и кожного зуда, может появится тогда, когда почечная недостаточность достигла уже финальной стадии.
Есть и противопоказания для проведения биопсии, например, если у человека функционирует только одна либо есть выраженные изменения со стороны свертывающей системы крови, которые могут вызвать осложнение в виде кровотечения. Во втором случае биопсия возможна только после коррекции нарушений – к процедуре пациента надо подготовить. Тем же, кто принимает препараты, разжижающие кровь, перед биопсией надо их отменить.
Как делается биопсия?
Для проведения биопсии пациент госпитализируется в стационар на 3-4 дня. В первый день сдает необходимые анализы и делает УЗИ почек. Нужно убедиться, что удовлетворительны коагулограмма и уровень тромбоцитов, оценить состояние почек.
Процедура взятия биоптата проводится на второй день в процедурном кабинете под местной анестезией и ультразвуковым контролем. Пациент ложится на живот, с помощью аппарата УЗИ изображение почки выводится на экран, чтобы врач мог точно выполнить манипуляцию. Как правило, проводится биопсия левой почки, чтобы минимизировать возможные операционные осложнения, поскольку справа находится печень. Вводится специальная игла, которая «забирает» столбик почечной ткани. Нам нужны два или три столбика (соответственно выполняются два или три прокола) в зависимости от количества используемых методов. Обязательны два метода: световая и иммунофлуоресцентная микроскопия. Третий метод, электронная микроскопия, используется только при подозрении на некоторые диагнозы.
После проведения биопсии, пациента возвращают в палату, где он соблюдает постельный режим в течении суток. На следующий день проводится УЗИ контроль, чтобы убедиться в отсутствии осложнений. Результаты морфологического исследования биоптата обычно готовы на третий-четвёртый день, и на их основании принимается решение о лечебной тактике. Когда требуется стационарное лечение, то сразу начинаем его. Если возможна амбулаторная терапия, то пациент выписывается с рекомендациями по лечению под контроль врача-нефролога по месту жительства.
Как часто и какие могу быть осложнения биопсии?
Я бы не сказала, что осложнения часты, но они бывают. Причина – анатомические особенности расположения и состояния сосудов почки. Полностью избежать их невозможно, даже при простой внутримышечной инъекции могут образовываться гематомы. Подавляющее большинство осложнений – легкие. Это небольшие гематомы, которые рассасываются самостоятельно. Крайне редко бывают большие гематомы, которые требуют дополнительного вмешательства. Это случается у пациентов с высоким уровнем креатинина. Соответственно, мы можем спрогнозировать наличие повышенных рисков заранее и подготовить пациента. Другое возможное осложнение — кровь в моче, которая также, как правило, регрессирует в течении суток.
Где можно сделать биопсию?
Как говорит профессор Столяревич, «Плохо сделанная биопсия хуже, чем ее отсутствие». Важно получить качественный материал, исследовать его правильными методами и точно интерпретировать результаты. Точный диагноз зависит не только от квалификации морфолога, но и от его кооперации с лечащим врачом – нефрологом. Ведь морфолог видеть только часть информации, важно соединить ее с другой, которую знает лечащий врач. Врач видит пациента, знает анамнез, результаты анализов. Получив результаты биопсии, Столяревич созванивается с врачами нашей больницы и других лечебных учреждений, чтобы получить дополнительную информацию и обсудить полученные данные.
Если пациент отправляет результаты биопсии самостоятельно, важно предоставить контакты лечащего врача. А также помнить, что материал для иммунофлуоресцентной микроскопии имеет очень короткий срок годности. Если мы делаем световую микроскопию, кусочек почечной ткани кладется в формалин, это значит, что препарат может храниться долго. Для иммунофлуоресцентной микроскопии нужна еще живая ткань, которая помещается в физраствор и может хранится не больше суток. Бывает обидно, когда человек сделал биопсию, подвергся инвазивной манипуляции, а материал оказался «испорченным». Процедуру придется повторить. Поэтому мы предлагаем делать биопсию у нас, сразу получить и анализ, и рекомендации по лечению.
Как сделать биопсию в ГКБ № 52?
Чтобы получить бесплатные медицинские услуги по ОМС, надо иметь направление из поликлиники (форма 057у) для консультации и госпитализации в ГКБ № 52. Записаться на прием в консультативно-диагностическое нефрологическое отделение (КДНО) по телефонам 8 (499) 196-22-48 и 8 (499) 196-18-84 ( будни с 9 до 19 часов). Врач-нефролог КДНО оценит необходимость биопсии и наличие противопоказаний, предложит дату госпитализации.
Как привезти заранее взятый материал на исследование в ГКБ №52?
Пациент может самостоятельно привезти материал в лабораторию. Лаборатория находится в 15 корпусе (патологоанатомическое отделение), вход с тыльной стороны здания. Документы: паспорт (копия первой страницы и регистрация) , полис ОМС ( копия с 2х сторон) и направление от врача на исследование.
Телефон ПАО 8 (499) 194-76-84 с 9.00 до 15.00.
Как сделать биопсию иногородним пациентам?
Биопсию у нас делают и пациенты из регионов. Уточнить возможность получить направление 057у в московскую ГКБ № 52 можно у врача в своем регионе. Также по программе «Москва столица здоровья» иногородние граждане могут оставить заявку на лечение в столице Лечение в Москве: плановая госпитализация иногородних пациентов.
Есть ли платные услуги?
Если человек хочет самостоятельно оплатить обследование и биопсию в нефрологическом отделении ГКБ№ 52 надо обратиться в отделение платных услуг по телефону +7 (495) 870-36-04 ежедневно с 9:00 до 20:00, кроме воскресенья. Важно предоставить максимум информации о своем состоянии, на основании которой врачи определят объем необходимых исследований и план действий. Можно начать с того, чтобы записаться на платный прием врача-нефролога КДНО по тем же телефонам.
Биопсия почки — инвазивный метод диагностики, суть которого сводится к забору из почки столбиков ткани диаметром ~2 мм с их последующим гистологическим, иммуногистохимическим, генетическим исследованием.
Биопсия почки является основным методом диагностики аутоиммунных заболеваний почек, таких как гломерулонефрит. Назначают выполнение биопсии почки, как правило, нефрологи и ревматологи, а выполняют урологи с помощью специального биопсийного пистолета под УЗИ – наведением.
Принципиальными моментами в биопсии почки являются: качество выполнения и, главное, экспертная оценка результатов квалифицированным патологом для точной постановки диагноза и правильного лечения.
Показания к проведению биопсии почек
Биопсия почек — это процедура взятия образца ткани, назначаемая врачом:
- для подтверждения/опровержения предположения о развитии нефротического синдрома;
- для определения степени и уровня развития гломерулонефрита;
- при обнаружении в анализах крови превышения показателей креатинина, мочевой кислоты, мочевины;
- при выявлении патологии на УЗИ или КТ;
- при подозрении на онкологическое заболевание
- при частых острых или хронических патологиях почек, причины которых до конца не выяснены;
Противопоказанием к выполнению биопсии почки является прием пациентом препаратов, нарушающих свертываемость крови.
Подготовка к биопсии
Перед проведением процедуры врач рассказывает пациенту о том, для чего и как будет проводиться процедура, а также какие осложнения она может вызвать. Также специалист задаст пациенту вопросы про имеющиеся заболевания и общее самочувствие, узнает есть ли у пациента аллергия на определенные лекарственные препараты. Если все в порядке, назначается дата проведения процедуры и подписывается разрешение на вмешательство.
За две недели до процедуры пациенту нужно отменить прием препаратов, разжижающих кровь и влияющих на ее свертываемость, с целью минимизировать риск появления кровотечения. К этим медикаментам относятся антикоагулянты, антиагреганты, нестероидные противовоспалительные средства. Некоторые диетические добавки также следует исключить из рациона. Это рыбий жир, чеснок, гинкго. Многие препараты может правильно оценить лишь доктор. Поэтому, во время подготовки перечислите лечащему врачу все медикаменты, которые вы принимаете или принимали в недавнее время. Учитывая эти данные, врач выберет оптимальный период для процедуры и скажет, после какого времени можно возобновить прием препаратов.
За несколько дней до проведения биопсии необходимо пересдать все анализы, в назначенный день необходимо отказаться от еды и питья, за день — очистить кишечник с помощью клизмы или слабительных средств. За несколько дней до биопсии пациенту рекомендуется анализы крови и мочи, чтобы доктор оценил состояние организма и его готовность к манипуляции.
Как проводится биопсия почки?
Процедура занимает около 30-40 минут. Биопсию делают под местным наркозом, если пациент сильно нервничает, ему дают седативные средства для уменьшения чувства страха и расслабления.
-
Во время процедуры пациента укладывают на живот, к нему подсоединяют датчики для измерения пульса и давления.
-
Для того, чтобы выбрать оптимальное место для биопсии, используется УЗИ или КТ. Это необходимо для того, чтобы не нарушить целостность окружающих тканей и сосудов.
-
Определив место взятия материала, врач обрабатывает его антисептиком. В этот участок вводится анестетик который снижает чувствительность. Когда лекарство подействует, врач делает небольшой разрез кожи. Водится игла для биопсии. Её движение контролируется с помощью ультразвука.
-
Во время процедуры врач помогает пациенту, разговаривает с ним и советует, как регулировать дыхание. Взяв необходимое количество материала, врач извлекает инструменты. На рану накладывается стерильная повязка.
-
После завершения подготовки пациенту производится местная анестезия, в области над почкой врач делает небольшой надрез, через который с помощью специального пистолета берется образец ткани. Во время процедуры врач будет давать пациенту указания о задержке дыхания, которые нужно неукоснительно соблюдать. В некоторых случаях врач может ввести контраст, это делается для того, чтобы сосуды и ткани было лучше видно.
Виды биопсии почек
Виды биопсии отличаются по способу взятия образца:
- чрескожная — взятие образца иглой под УЗИ-наведением;
- открытая — берется во время открытой операции, например, при удалении опухоли;
- уретроскопическая — выполняется если в мочеточнике или почечной лоханке обнаружены камни, выявлена аномалия или заболевания верхних мочевых путей, а также, если почка была трансплантирована. Уретероскоп проводится через мочеточник в лоханочную систему почки. Это дает возможность обзора органа и забора ткани. Такой метод применяется для детей и беременных. Манипуляция требует выполнения спинальной анестезии или наркоза;
- лапароскопическая — проводится через несколько отверстий в передней брюшной стенке. Применяется при нарушениях свертывающей системы крови, а также пациентам с одной функционирующей почкой. Через троакар к почке подводится камера и осветитель.
После процедуры
После биопсии почки в течение нескольких часов пациента наблюдает медицинский персонал, проверяя давление, пульс и другие показатели. Если никаких осложнений нет, после того, как действие наркоза закончится, пациента могут отпустить домой. Взятый материал отправляется в лабораторию для проведения исследований, по мере готовности результат сообщается пациенту.
В послеоперационный период для пациента рекомендуется:
- соблюдать постельный режим в течение 6 часов после процедуры;
- обильное питье в первые сутки после процедуры;
- воздержание от физических нагрузок на протяжении 2-4 дней, от подъема тяжестей — в течение 2 недель.
В нашем стационаре есть все условия для получения максимально достоверных результатов биопсии почки.
Получить консультацию и определить индивидуальную тактику лечения заболевания можно у врачей нашего онкологического отделения № 2 (урология) Клиники высоких медицинских технологий им. Н. И. Пирогова Санкт-Петербургского государственного университета.
Что такое биопсия почек: подготовка и проведение процедуры
Исследование состояния почек методом биопсии
Биопсия почек – это диагностический метод исследования. Он позволяет отследить изменение в органе и его строении. С помощью процедуры исследуют слои почечной оболочки. Некоторые морфологические исследования бывают безопасными. Другие опасны осложнениями, проводятся в операционной, требуют специально подготовки. Биопсия почки считается небезопасной процедурой. Методика проведения процедуры появилась в прошлом веке. С тех пор оснащенность стационаров улучшилась. Добавилась возможность отслеживать инструмент во время исследования с помощью УЗИ.
Представление о нефробиопсии
Процедypa помогает определить прогноз при патологии. В зависимости от результата отменяется или назначается иммуносупрессивное лечение. Исследование проводится в стационарах или отделениях больницы. Направление выписывает врач нефролог.
Разновидности биопсии
Биопсия почки — основной способ диагностики. С ее помощью можно поставить верный диагноз, назначить корректное лечение. Другие неинвазивные методы и анализы часто дают неверные результаты. Различают 5 видов процедуры, в зависимости от способа получения материала:
- Чрескожная пункционная биопсия почки. Инструмент помещается в орган, процедypa контролируется ультразвуком. Наиболее популярный метод.
- Лапароскопическая нефробиопсия. Забор материала проводится через прокол в коже. Контролируется исследование с помощью видеокамеры.
- Трансяремная нефробиопсия почек. Назначается, когда нельзя применять наркоз, при патологии дыхательной системы, нарушении гемостаза, излишнем весе. Пункцию почки проводят через почечные вены.
- Открытая. Забор части почки делается во время операции. Данный вид исследования применяется при наличии опухоли.
- Эндоскопическая биопсия. Инструмент вводится через мочеточник. Применяется после пересадки органа, у пожилых, детей и беременных.
Показания и противопоказания
Основная цель назначения биопсии – возможность постановки верного диагноза, отражающего системное заболевание или почечную патологию. Прокол позволяет контролировать течение процесса, помогает определить, требуется ли организму трaнcплантация почки. С помощью данного метода можно подобрать правильную терапию и вести научно-исследовательскую деятельность при изучении болезней органа.
Для проведения биопсии почки показания таковы:
- Нефротический синдром.
- Когда почка задействована в каком-либо воспалительном или аутоимунном процессе в организме.
- В моче есть белок или другие изменения.
- Гипертензия артерий вторичная.
- Почечная недостаточность в период обострения.
- Структурные изменения почечных кaнaльцев.
Диагноз «Острая почечная недостаточность» можно поставить без биопсии. Процедypa поможет установить причину поражения. Иногда она бывает понятна, например, при отравлении пациента грибами или ядами. При тубулярном некрозе, подростковым гломерулонефрите без биопсии чаще всего не обойтись.
Показание к исследованию бывает, когда гемодиализ или иное патогенетическое лечение не улучшают самочувствие больного. Биопсия почек при гломерулонефрите позволяет определить, насколько развилось воспаление.
Противопоказания бывают относительными и абсолютными. К последнему виду относятся:
- тромбы, которые расположены в почечных венах;
- гнойнички, экзема в месте забора пункции;
- острое заболевание, вызванное инфекцией;
- одна почка у человека;
- политоксикоз;
- нарушение свертываемости крови;
- воспаление органа или клетчатки, носящее гнойный характер;
- злокачественное новообразование;
- туберкулезное поражение;
- сердечная недостаточность правого желудочка;
- кома;
- аневризма артерии органа (почечной);
- психическое заболевание.
Не желательна пункция органа при поликистозе, атеросклерозе артерий, миеломе, гипертонии, наличии образований, необычной подвижности почек, некоторых васкулитах, а также при тяжелой почечной недостаточности.
Проведение процедуры
Изначально нефролог спрашивает о заболеваниях, узнает, есть ли аллергия, об операциях, проведенных ранее. Многие больные не знают, что такое биопсия почек. Поэтому перед исследованием доктор описывает процедуру, связанные с ней риски. Пациент озвучивает вопросы, затем подписывает согласие о хирургическом вмешательстве.
Подготовительный этап
Подготовка начинается за 2 недели. За 10-14 дней отменяется употрeбление нестероидных противовоспалительных препаратов и кроверазжижающих средств. Перед исследованием нельзя есть, между последним приемом еды и биопсией должно пройти не меньше 8 часов. Восприимчивым людям могут назначить слабые транквилизаторы.
За несколько дней до прокола у исследуемого будут брать кровь для общего и биохимического анализа, сдается моча, делается коагулограмма, а также флюорография, УЗИ почек и ЭКГ. При болезнях других органов назначается консультация у узкого специалиста.
Исследование могут проводить в стационаре, процедурном кабинете или в операционной. Длится прокол почки в среднем 30 минут, чаще всего используется местная анестезия. Если пациент эмоционально нестабилен, вводится препарат, погружающий его в полусон. При этом человек находится в сознании. Общий наркоз делается в исключительных случаях.
Каждый больной должен знать, как делают биопсию почки. Человека просят лечь спиной кверху, лицо оказывается внизу. Под брюшину или гpyдь помещается подушка или валик. Они позволяют поднять орган ближе к спине. В течение всего исследования контролируют пульс и артериальное давление.
Определить местонахождение почки можно под 12 ребром по задней подмышечной линии с помощью ультразвука или другого метода. Кожу в месте прокола смазывают антисептиком, вводится обезболивающее.
Затем делают надрез длиной в 2-3 мм, через него вводится инструмент по траектории, определенной ранее. При разрезе, а также пункции обычно не больно. Когда игла оказывается под кожей, пациента просят сделать вдох и не дышать 30-45 секунд. Это позволяет зафиксировать органы в одном положении.
Игла проникает в орган на 0,1-0,2 см. Забор материала происходит автоматически. После инструмент извлекают. На кожу повторно наносится антисептик, сверху кладется повязка.
Восстановительный период и осложнения
После процедуры рекомендуется отдыхать 10-12 часов. В эти часы измеряется пульс и давление, врачи смотрят, есть ли кровь в моче.
Есть после процедуры можно сразу, нужно пить больше жидкости. Спина иногда слегка болит, при необходимости назначают aнaльгетики. Если нет осложнений и показатели нормальные, больного выписывают в этот же день.
После исследования нельзя поднимать тяжести 2 недели, на несколько дней нужно ограничить физическую активность.
Возможные последствия после процедуры:
- Обструкция мочевыводящих путей.
- Разрыв почки или различные кровотечения в области чашечки или в лоханке.
- Гематома подкапсульная или паранефральной клетчатки.
- Повреждение остальных органов, сосудов, а также инфекции, воспаления и гнойный паранефрит.
Оценка результатов
Забранный материал исследуется 1-2 дня. Иногда результаты готовы только через 1,5-2 недели. Нормой считаются случаи, если нет проявления опухолей, инфекций, воспалений и рубцов. Наличие последних чаще указывает на гломерулонефрит и иные патологии.
Аномальный результат указывает на изменение почечной структуры, инфицирование, системные нарушения соединительной ткани, недостаток кровотока. Если исследуют пересажанную почку, отрицательный итог говорит об ее отторжении.
Преимущества и недостатки
Как и у любого метода исследования, у биопсии есть свои плюсы и минусы. К положительным сторонам диагностической манипуляции можно отнести следующее:
- простота подготовки к процедуре;
- информативность;
- является наиболее достоверным и точным методом диагностики.
Риски процедуры включают в себя такие пункты:
- большой список противопоказаний;
- высокая стоимость;
- возможность осложнений после проведения.
Многие задумываются, сколько может стоить прокол почки. Цена зависит от города и от самого учреждения. Так в небольших населенных пунктах, процедypa обойдется в 1500-2000 рублей. В столице в государственных учреждениях цены начинаются от 2500 руб. (поликлиника МИД России), 3000 руб. в Городской клинической больнице №67 им. Л. А. Ворохобова, 4000 руб. исследование будет стоить в Федеральном клиническом центре высоких медицинских технологий федерального медико-биологического агентства, ФГБУ.
В частных учреждениях цены начинаются от 5000 руб. (клиника «МединаМед»). Доходить в Москве они могут до 60000 руб., средняя стоимость равняется 25-30 тыс. руб. В Санкт-Петербурге максимальная цена исследования 25000 руб., в частных клиниках можно найти варианты за 10, 7 тыс. руб. и ниже. Наименьшая цена процедуры 1300 рублей в ленинградском онкодиспансере.
Подавляющее большинство мнений о биопсии хорошее. Люди говорят об отсутствии значительного дискомфорта во время процедуры, быстром проведении и коротком восстановительном периоде. Ниже приведены 3 отзыва.
Все происходит быстро, процесс отточен до мелочей, людей много. С нашего отделения было 4 человека, и множество пациентов с других. На каждого больного выделяется по 15 минут. Кладут на живот, место прокола обpaбатывают антисептиком, затем обезболивающим.
Дальше непонятно, так как боль не чувствуется, только копошение в спине. После процедуры сутки покоя в отделении, кололи кровоостанавливающие. На следующий день делают УЗИ. Через неделю будут готовы результаты гистологического исследования.
Биопсию выполняют с целью диагностики. Болезненные ощущения минимальны. Чаще пациенты описывают момент выстрела иглы как тупой толчок.
Исследование безболезненно. При вводе иглы чувствуется как будто щипок. Если нервничаешь, могут предложить успокоительное. Лучше его принять.
Нервничала перед самой процедурой. Нашла сайт, где можно посмотреть фото и видео биопсии. Немного успокоилась, выглядит это не страшно.
Судя по отзывам, исследование безболезненное, не требует особой подготовки и легко переносится большинством людей.
Биопсия почки – это информативный метод исследования, позволяющий поставить диагноз, узнать характер патологии, назначить верное лечение. Как и любое хирургическое вмешательство, эта процедypa связана с рисками. Но в связи с развитием технологий опасности от прокола минимизированы, больные легче переносят биопсию почки.
Как подготовиться к биопсии почки
Биопсия почки — это диагностическая манипуляция, во время которой врач высекает почечные ткани для микроскопического и макроскопического исследования. Процедypa проводится только при абсолютных показаниях в специализированном нефрологическом отделении.
Существуют два метода проведения биопсии почек: пункционная биопсия и операционная биопсия.
- Пункционная биопсия почки выполняется в диагностических целях с помощью пункционной иглы и под контролем УЗИ-аппарата.
- Операционная биопсия — это метод взятия образца тканей почки непосредственно во время проведения операции на органе для оценки морфологической картины и подтверждения диагноза.
Читать еще: Описание и фото рака челюсти: его причины, симптомы и способы распознавания
Биопсия почки — это операционное вмешательство, которое требует определенной подготовки как со стороны врача, так и со стороны пациента.
Для чего делается биопсия почки?
Биопсия почки проводится при хронических заболеваниях верхних отделов мочевыделительной системы, когда другие диагностические методы исследования неэффективны (УЗИ, анализ мочи, КТ), и позволяет:
- установить диагноз системного заболевания, которое поражает почки (системная красная волчанка, дерматомиозит, амилоидоз) или диагноз заболевания, которое ограничивается только поражением почек (подострый гломерулонефрит, хронический пиелонефрит);
- подобрать лечение в зависимости от стадии патологического процесса;
- прогнозировать развитие заболевание и оценить показания к возможной трaнcплантации почки;
- уточнить диагноз некоторых наследственных заболеваний;
- оценить состояние пересаженной почки.
Также, как дополнительный диагностический метод, врач может назначить пункционную биопсию почки при выявлении:
- крови (гематурия) в общем анализе мочи;
- следов белка (микроальбуминурия, протеинурия) в общем анализе мочи;
- признаков почечной недостаточности, что проявляется накоплением токсических продуктов метаболизма в крови (креатинин, мочевина).
Однако, эти отклонения от нормы не являются абсолютными показателями к проведению данной процедуры. Решение о проведении пункционной биопсии почки принимает лечащий врач на основаниях всесторонней оценки данных анамнеза болезни, проведенных обследований и состояния больного.
Противопоказания к проведению биопсии почки
- отсутствие одной почки;
- нарушение свертывающей функции крови;
- поражения почечной артерии (тромбоз, аневризма);
- правожелудочковая недостаточность;
- диагностированная опухоль почки;
- поликистоз почек;
- пио- и гидронефроз.
- тяжелая артериальная гипертензия;
- системный атеросклероз;
- узелковый периартериит;
- миеломная болезнь.
Подготовка к проведению биопсии почки
Перед выполнением пункционной биопсии почки потребуется подготовка. Пациент должен предоставить врачу полный список диетических добавок, лекарственных препаратов, которые он принимает, сообщить о наличии аллергии. Лечащий врач назначает диагностические обследования: общий анализ мочи и крови, анализ на групповую принадлежность крови и резус-фактор, коагулограмму (состояние свертывающей функции крови).
В обязательном порядке по назначению лечащего врача отменяются препараты, которые снижают свертывающую функцию крови:
- антикоагулянты за 14 дней до проведения процедуры (варфарин, гепарин, эноксапарин);
- антиагреганты за 7 дней до проведения процедуры (аспирин, клопидогрель, аспирин-кардио);
- нестероидные противовоспалительные препараты за 7 дней до проведения процедуры (ибупрофен, парацетамол, нимесулид);
- пищевые и диетические добавки, которые содержат рыбий жир, чеснок, гинкго билоба.
В день проведения биопсии почки полностью отменяется прием жидкости, а последний прием пищи должен быть не раньше, чем за 8 часов до манипуляции.
Как делается биопсия почки?
Для седации пациенту вводят легкое успокоительное средство (седуксен, сибазон). После этого пациента просят лечь на спину для максимального перемещения почек к поверхности кожи. Процедypa проводится под контролем УЗИ-аппарата, с помощью которого определяют точное место прокола. Далее место прокола обpaбатывают антисептиком. Местная анестезия осуществляется введением 0.25% раствора новокаина. После приведения в действие обезболивания на ранее зафиксированном месте скальпелем делается небольшой разрез кожи и мягких тканей, через который в паренхиму почки вводится аспирационная игла. Весь процесс контролируется аппаратом УЗИ.
Непосредственно во время забора почечной паренхимы пациента просят задержать дыхание до появления щелчка, который свидетельствует об окончании забора образца ткани. Таких заборов может быть произведено несколько, в зависимости от вида патологии. По окончанию врач останавливает кровотечение, зашивает рану, а кожу еще раз обpaбатывает антисептиком.
Длится биопсия почки в среднем около часа. Домой пациент сможет отправиться через несколько часов, после того, как будут сделаны общий анализ крови и мочи, УЗИ и взвешен риск возникновения осложнений.
Возможные осложнения после биопсии почки
В большинстве случаев осложнения после проведения биопсии почки не наблюдаются, но с частотой в среднем около 3.5% возникают такие последствия:
- кровотечение дольше 24 часов с образованием гематомы;
- кровотечение дольше 3 суток с образованием инфаркта почки;
- инфицирование гематомы с образованием гнойного пиелонефрита.
О возникновении кровотечения свидетельствуют болевые ощущения в пояснице, примесь крови в моче, падение кровяного давления, понижение гемоглобина в общем анализе крови, поэтому пациент в первые 3 суток должен следить за уровнем артериального давления, количеством и качеством мочеиспускания, температурой. Чтобы предупредить возникновение осложнений нужно с точностью выполнять указания врача перед и во время операции, пить достаточное количество воды и удерживаться от физической деятельности после операции.
Внимание! Данная статья размещена исключительно в ознакомительных целях и ни при каких обстоятельствах не является научным материалом или медицинским советом и не может служить заменой очной консультации с профессиональным врачом. За диагностикой, постановкой диагноза и назначением лечения обращайтесь к квалифицированным врачам!
Биопсия почки: показания, методы ее проведения, стоимость
Биопсия почек – информативная диагностическая процедypa, предполагающая получение биоматериала из почек с помощью специального шприца.
В результате гистологического изучения тканей специалисты получают полную картину заболевания, точный диагноз и нужный план лечения.
Диагностическая процедypa вроде почечной биопсии показана в следующих случаях:
- Сложные мочевыводящие инфекционные патологии;
- Хронические либо острые патологические процессы в почках, имеющие неясную этиологию;
- Наличие белка и крови в составе мочи;
- Стремительно развивающийся гломерулонефрит;
- Присутствие в крови шлаков азотистого происхождения вроде креатинина, мочевины или мочевой кислоты;
- Для уточнения разного рода почечных патологий, обнаруженных при ультразвуковом исследовании или компьютерной томографии;
- При наличии подозрений на нефротический синдром либо рак почки;
- С целью установления стадии развития и степени тяжести почечных патологических процессов;
- Нестабильная, нарушенная деятельность имплантированной почки;
- С целью оценки терапевтической эффективности назначенного лечения.
Противопоказания
Но даже такая полезная во всех отношениях процедypa, обладающая высочайшей информативностью, имеет специфические противопоказания.
Категорически недопустимо проводить почечную биопсию, если:
- Имеется лишь одна функционирующая почка;
- Проблемы с кровесвертываемостью;
- Аллергическая реакция на новокаин и препараты на его основе;
- Обнаружена почечная опухоль;
- Выявлена аневризма артерии почки;
- Обнаружен почечный кавернозный туберкулез, венозный тромбоз или гидронефроз.
Кроме того, относительно противопоказана почечная биопсия при миеломных процессах, тяжелых формах диастолической гипертонии, последних этапах атеросклероза, почечной недостаточности, нефроптозе или патологической почечной подвижности, узелковом периартериите и пр.
Существует несколько методов проведения почечной биопсии:
- Открытая форма. Эта методика предполагает проведение операции с разрезом над местом расположения почки, в процессе которой из органа берется кусочек ткани. Обычно открытая методика применяется, когда нужно удалить объемную часть ткани. На сегодня открытую биопсию часто проводят лапароскопическим способом, который отличается меньшей травматичностью.
- Чрескожная биопсия – осуществляется посредством специализированной иглы, которая вводится через кожный слой над почкой под рентгеновским или ультразвуковым контролем. Иногда эта процедypa сопровождается применением контрастного вещества, чтобы визуализировать почку и сосудистую сеть в месте прокола.
- Трансяремная биопсия. Эта процедypa проводится с применением катетера, который запускается в почечную вену. Такая методика получения биоптата рекомендована для лиц, имеющих нарушения кровесвертываемости, ожирение или дыхательную недостаточность.
- Уретроскопия с забором биоптата обычно проводится пациентам с конкрементами в мочеточниках или почечных лоханках. Уретроскопию проводят в операционных условиях с использованием общей либо спинальной анестезии. Через уретру вводится длинная гибкая тончайшая трубочка, проходит по мочевыводящим путям до почек, где и осуществляется забор биоптата.
Конкретный метод выбирается индивидуально в случае с каждым пациентом. Специалист учитывает состояние больного, цели биопсии, возможности клиники и прочие факторы.
Подготовка к процедуре
Врач предварительно сообщает о подозрениях, ставших причиной проведения биопсии, и обязательно сообщает пациенту о вероятных рисках и осложнениях.
Между медучреждением и пациентом заключается договор о согласии на проведение диагностической процедуры, в котором сказано об осведомленности больного о возможных последствиях.
Затем врач выясняет наличие патологий, аллергических реакций и непереносимости медикаментов, а также расспрашивает больного о принимаемых им препаратах.
В целом подготовка к диагностике предполагает следующее:
- За 1-2 недели до процедуры необходимо прекратить употрeбление препаратов вроде Ривароксабана, Аспирина, Дабигатрана и прочих медикаментов, обладающих кроверазжижающим действием;
- Пройти лабораторное исследование крови и мочи для исключения инфекционных поражений и определения противопоказаний;
- За 8 часов до процедуры прекращают есть, а перед процедурой не употрeбляют жидкость;
- Прекратить употрeбление обезболивающих медикаментов типа Напроксена, Ибупрофена, поскольку эти препараты влияют на кровесвертываемость и повышают вероятность кровотечения.
Как делается биопсия почек?
Диагностическая процедypa проводится в стационарных условиях в операционной или процедурной комнате.
Общая длительность процедуры составляет порядка 30 минут.
Пациента располагают на кушетке животом вниз, подключают аппаратуру для контроля пульса и давления. Все манипуляции контролируются магнитно-резонансным или компьютерным томографом, рентгеном или ультразвуковым аппаратом.
- Сначала специалист определяет место введения биопсийной иглы, область вокруг которого обкалывают анестетиками.
- Затем пациента просят сделать глубокий вдох, задержав дыхание почти на минуту (45 сек.).
- Когда происходит введение иглы больные отмечают давящее ощущение, после чего отчетливо слышат звук щелчка, что говорит о проколе почечной оболочки и заборе материала. Просто при заборе биоптата применяется специальный прибор, который в момент затягивания биоматериала производит щелкающий звук.
- Когда врач соберет необходимое количество биоптата, иглу аккуратно вынимают.
- Место прокола обpaбатывают антисептиком и закрывают повязкой.
Когда прекращается действие анестетиков, возникает болезненный дискомфорт в месте прокола. Через несколько часов после забора биоптата у пациента исследуют мочу на предмет обнаружения кровяных примесей.
Читать еще: Аденомиоз матки что это такое доступным языком с фото
Биопсия почек при гломерулонефрите
Широко применяется биопсия при появлении подозрений на гломерулонефрит.
Только биопсия может прояснить картину состояния почек и определить точный характер изменений, произошедших в тканях органа.
Микроскопическое, иммунофлюоресцентное и морфологическое исследование биоптата позволяет определить наличие поражений различной классификации:
- Наличие незначительных изменений с минимальной тканевой деструкции;
- Нефрит мембранозного типа, для которого характерна эпителиальная почечнокaнaльцевая дистрофия;
- Гломерулонефрит пролиферативного характера, сопровождающийся интракапиллярной пролиферацией;
- Хронический прогрессирующий гломерулонефрит, который считается завершающей стадией патологии.
Обычно поводом для почечной биопсии становятся изменения в качественных или количественных характеристиках мочи и ее структуры. По результатам биопсии врачу проще подобрать самую эффективную схему лечения, способствующую скорому выздоровлению пациента.
Результаты
Результаты обычно готовы через несколько дней, однако, если целью биопсии было выявление инфекционно-воспалительного процесса, то пациенту придется ждать результатов до 10-14 суток.
Результаты считаются нормальными, когда отсутствуют любые проявления опухолей, инфекционных поражений, рубцов и воспалений.
Если в ходе биопсии были обнаружены рубцовые изменения, то это может указывать на системные поражения, пиелонефрита, гломерулонефрита и прочих патологий.
Осложнения
Среди наиболее распространенных осложнений при проведении почечной биопсии специалисты выделяют:
- Внутренние кровотечения, которые со временем самостоятельно проходят (в 10%);
- Серьезные кровотечения, требующие переливания крови (менее 2%);
- Сильное кровотечение, для устранения которого необходима операция (вероятность 0,0006%);
- Потеря почки (менее 0,0003%);
- Паранефрит гнойного характера, сопровождающийся воспалительными поражениями околопочечных липидных тканей;
- Пневмоторакс;
- Мышечные кровотечения;
- Прорыв в нижней части почки;
- Инфекционные осложнения.
Восстановительный период
Согласно врачебным рекомендациям, когда больного отпустят домой, ему необходимо придерживаться определенного режима:
- В течение 2-3 дней соблюдать пocтeльный режим;
- Употрeблять больше питья;
- На двое суток исключить физические нагрузки;
- Для профилактики принимать антибиотики и гемостатики;
- На пару-тройку месяцев отказаться от занятий спортом и поднятия тяжестей.
Отзывы пациентов
Инга:
Так случилось в жизни, что заболела у меня почка. Прошла кучу врачей, дошла до онколога, который и нашел в почке новообразование, после чего назначил биопсию. Пришла в клинику, меня провели в палату, где разделась и надела операционный халат. Потом операционная, наркоз и больше ничего не помню. Поскольку делали с общим наркозом, то боли не было. Но у меня по показаниям можно было только открытую биопсию проводить. Все прошло удачно, осложнений никаких.
Виктория:
Сильно боялась, когда назначили биопсию, да еще наслушалась, что процедypa эта очень болезненная. А одна знакомая вообще сказала, что после почечной биопсии еще неделю плохо себя чувствовала и почка болела. Но на деле все получилось совсем не так. Сделали в вену укол, и я уснула. Когда в себя пришла, уже все манипуляции были окончены. Поэтому не так все страшно, как описывают.
Цена анализа и где его можно пройти?
Процедуру почечной биопсии можно пройти в высококвалифицированных клиниках, республиканских профильных медцентрах и столичных многопрофильных больницах, имеющих профессиональный и обученный персонал.
Средняя стоимость пункционной чрескожной биопсии составляет порядка 2300-24000 рублей.
Видео о том, как и когда применяется биопсия новообразований почек:
Как проводится биопсия почки?
Информация для пациентов по процедуре биопсии почки
Что такое биопсия почки?
Биопсия почки – процедypa, включающая взятие небольшого кусочка почечной ткани для исследования под микроскопом. Клинический патолог (в России патологоанатом) – врач, специализирующийся на диагностике заболеваний. Он исследует образец ткани почки в лаборатории. Патологоанатом ищет признаки заболевания почек или инфекции. Если почка была трaнcплантированная и не функционирует, биопсия почки может помочь определить причину.
Специалисты, выполняющие биопсию почки в больнице или амбулаторном центре:
- нефролог – врач, специализирующийся на лечении заболеваний почек
- уролог – врач, специализирующийся на лечении урологических и ceкcуальных проблем
- хирург-трaнcплантолог – врач, специализирующийся на пересадке органов
- интервенционный радиолог – врач, который выполняет процедуры с использованием оборудования для визуализации
Зачем проводится биопсия почки?
Биопсию почки проводят для оценки любого из следующих состояний:
- Гематурия – кровь в моче (может быть признаком заболевания почек или других проблем с мочеиспусканием)
- Альбуминурия – состояние, при котором в моче содержится больше нормы белка, называемого альбумином (может быть признаком заболевания почек).
- Изменения в функции почек, вызвающие скопление отходов в крови.
Показания к проведению биопсии почки
- Затяжная острая почечная недостаточность;
- изолированная протеинурия невыясненной этиологии;
- нефротический синдром;
- постоянная или эпизодическая гематурия невыясненной этиологии (несмотря на выполнение визуализирующих исследований и цистоскопии);
- подозрение на нефропатию при системных заболеваниях — системная красная волчанка, болезнь ассоциированная с антителами к базальной мембране (болезнь Гудпасчера), гранулематоз с васкулитом (Вегенера), IgA ассоциированный васкулит (старое название — пурпура Шенлейн-Геноха), ревматоидный артрит;
- нарушение функции трaнcплантированной почки — острое отторжение, острая ишемическая почечная недостаточность, медикаментозная нефропатия, вызванная циклоспорином или такролимусом, острый интерстициальный нефрит, острая гломерулопатия или васкулопатия.
Противопоказания к проведению биопсии почки
- Отсутствие одной почки,
- тяжелая артериальная гипертензия,
- поликистоз почек,
- гнойные изменения почек или окружающих их тканей,
- гидронефроз (учитывая возможность возникновения мочевой фистулы или развития пионефроза),
- пионефроз,
- новообразования почек (учитывая риск диссеминации и возможность кровотечения),
- множественные аневризмы почечных артериол,
- анемия тяжелой степени (относительное противопоказание — можно скорректировать перед манипуляцией),
- геморрагический диатез (АЧТВ >1,5 × верхней границы нормы; МНО >1,5, тромбоциты
Что должен делать человек за несколько дней до процедуры?
- беседа с врачом
- организация поездки домой после процедуры (нельзя будет садиться за руль)
Беседа с врачом
Пациенты должны поговорить со своим лечащим врачом об имеющихся у них заболеваниях, а также обо всех лекарствах, витаминах и добавках, которые они принимают:
- аспирин или лекарства, которые содержат аспирин
- нестероидные противовоспалительные препараты, такие как ибупрофен и напроксен
- разжижители крови
- лекарства от артрита
Пациенты должны также сообщить своему врачу о любой аллергии на лекарства или продукты питания.
Врач должен обсудить риски, связанные с процедурой. А пациент может задавать вопросы или высказывать опасения. За две недели до биопсии врач может посоветовать пациенту прекратить прием определенных лекарств, увеличивающих риск кровотечения после биопсии почки. Врач также может запретить запретить есть или пить что-либо за 8 часов до биопсии.
Организация поездки домой после процедуры
По соображениям безопасности пациенты не могут водить машину в течение 24 часов после процедуры, так как получают успокоительное и местную анестезию непосредственно перед процедурой.
Что ожидать пациенту в день биопсии почки?
Пациент должен прибыть за 1,5- 2 часа до биопсии почки, чтобы успеть на несколько предварительных процедур:
- Подписание информированного добровольного согласия пациента
- Проверка анализов крови
- Постановка внутривенных лекарств
Подписание формы согласия
Медицинский работник попросит пациента подписать форму информированного добровольного согласия. Там будет указано, что он понимает риски, связанные с процедурой и предоставляет врачу и учреждению разрешение на проведение биопсии почки.
Наличие анализов крови
Незадолго до процедуры медицинский работник берет анализы крови и мочи, чтобы убедиться, что у пациента нет противопоказаний.
Введение внутривенных лекарств
Пациенту поставят в вену лекарства, включая седативные.
Как проводится биопсия почки?
Процедypa обычно занимает около часа и включает следующие детали:
- Пациент лежит на животе на диагностическом столе. Под спину подкладывается твердая подушка. Пациенты с трaнcплантированной почкой лежат на спине.
- Медсестра поставит пациенту успокоительное в вену.
- Врач отметит точку попадания иглы под кожу. Область пункции дезинфицируется и обpaбатывается и вводится местный анестетик от боли.
- Затем врач использует методы визуализации (ультразвук) для направления иглы биопсии в почку. Иногда врач использует компьютерную томографию или магнитно-резонансную томографию для направления иглы в почку.
- Врач попросит пациента задержать дыхание и не совершать никаких движений. Затем вставляется игла для биопсии и берется почечная ткань. Когда врач выполняет биопсию, инструмент издает щелчки или хлопки. Врач может вставлять иглу три или четыре раза. Пациентам чаще всего нужно задерживать дыхание на 30 секунд или чуть дольше для каждой вставки.
Для пациентов с кровотечением используют лапароскоп – тонкую трубку с видеокамерой. Эта операция требует общей анестезии. Хирург делает небольшой разрез в спине и вставляет лапароскоп, чтобы увидеть почку.
Видео биопсии почки
Что делают после процедуры биопсии почки?
После биопсии почки пациенту необходимо:
-
Лежать на спине в клинике или больнице в течение нескольких часов (обычно 6) . В течение этого времени персонал будет следить (проводить мониторинг) за артериальным давлением, пульсом, мочой и результатами анализа крови.
Читать еще: Анастрозол
Каковы риски биопсии почки?
- Кровотечение – наиболее частое осложнение биопсии почки (из почки или места прокола). Редко требует переливания крови.
- Инфекция – редкое осложнение биопсии почки. Врач назначает антибиотики для лечения.
Осложнения после биопсии почки
Если после процедуры возникают следующие осложнения, следует немедленно обратиться к врачу:
- Невозможно мочиться.
- Частое или неконтролируемое мочеиспускание.
- Ощущение жжения при мочеиспускании.
- Моча темно-красная или коричневая. Розовая или слегка мутная моча считается нормальной в течение 24 часов после процедуры
- Кровь или гной из места биопсии (через повязку).
- Усиливающаяся боль в месте прокола.
- Повышение температуры.
- Ощущение слабости или головокружения.
- Пневмотракс. При неправильном выполнении прокола игла может попасть в плевральную полость и вызвать скопление в ней воздуха. Такое осложнение требует специального лечения.
Биопсия почки не всегда даёт точные результаты. Поэтому дополнительно могут понадобиться анализы крови и мочи, МРТ, КТ, УЗИ или рентген почки. Биопсия почки также может дать ложноотрицательный результат.
Где делают биопсию почки
Это достаточно сложная процедypa, требующая наличия в клинике соответствующих специалистов, специального оборудования и больничных палат. Поэтому она проводится в крупных государственных или частных клиниках.
Сколько стоит биопсия почки
В Росиии наблюдается большой разброс в цене на эту медицинскую услугу. Цены на биопсию почки начинаются от 3000 рублей и до 41000 тыс. руб. в зависимости от города, клиники и степени сложности.
Можно ли сделать биопсию почки бесплатно по полису ОМС?
Да, данная услуга может быть оказана в рамках программы ОМС. На плановое обследование можно записаться при наличии направления из центральной районной больницы, паспорта, полиса ОМС и СНИЛС. На практике зачастую пациенты сталкиваются со сложностями или длительными очередями на получение бесплатной процедуры. В этом случае придется обращаться в государственную или частную клинику или диагностический центр по договору платного обслуживания.
Биопсия почки — подготовка, проведение и риски связанные с биопсией почек
Биопсия почки – это диагностическая процедypa, во время которой врач берет небольшой образец почечной ткани для проведения анализов.
Врач может порекомендовать биопсию почки для уточнения диагноза, определения тяжести заболевания или периодического мониторинга эффективности лечения.
Биопсию также могут назначить после трaнcплантации почки, если по какой-то причине пересаженный орган плохо работает.
Чаще всего врач проводит биопсию почки при помощи длинной тонкой иглы, которую вводят сквозь кожу – это называется чрескожной биопсией почки. Устройства для визуализации, такие как аппарат УЗИ или КТ, позволяют следить за процессом и направлять иглу точно к цели.
Для чего делают биопсию?
Биопсию почки могут проводить по таким причинам:
• Диагностика некоторых заболеваний почек.
• Помощь в разработке плана лечения, основанного на состоянии почек.
• Определение скорости прогрессирования заболеваний почек.
• Определение степени повреждения почек при той или иной болезни.
• Контроль эффективности лечения болезней почек.
• Выяснение состояния пересаженной почки.
Врач может назначить биопсию почки, основываясь на результатах анализов мочи или крови, которые показали:
• Кровь в моче (гематурия), связанная с проблемами в почке.
• Белок в моче (протеинурия), которая сопровождается другими симптомами со стороны почек.
• Почечная недостаточность, которая приводит к накоплению токсичных продуктов обмена в крови.
Тем не менее, не каждому человеку с такими проблемами нужна биопсия почки. Врач будет принимать решение с учетом ваших симптомов, результатов обследования и общего состояния здоровья.
Риски, которые связаны с процедурой
Обычно чрескожная биопсия почки безопасна.
Но в редких случаях возможны осложнения:
• Кровотечение. Наиболее распространенным осложнением этой процедуры является появление крови в моче (гематурия). Кровотечение обычно прекращается через пару дней. Серьезное кровотечение, которое требует переливания крови, встречается после биопсии почки крайне редко. В некоторых случаях необходимо хирургическое вмешательство, чтобы остановить кровь.
• Боль. Боль в месте биопсии – это обычное явление после процедуры, но она, как правило, проходит через несколько часов. Для купирования боли врач назначит aнaльгетики.
• Артериовенозный анастомоз. Если во время биопсии игла случайно повреждает стенки соседней артерии и вены, то может сформироваться аномальное соединение между двумя кровеносными сосудами. Чаще всего такой анастомоз не вызывает никаких симптомов и закрывается сам по себе.
• Другие. Редко может возникать скопление крови (гематома) вокруг почки, которое инфицируется. Такое осложнение лечат антибиотиками или хирургическим путем.
Подготовка к биопсии почки
Перед биопсией почки вам нужно поговорить со своим врачом, чтобы узнать все риски и нюансы предстоящей процедуры. Следует задать все интересующие вопросы, чтобы осознавать, на что вы соглашаетесь.
Когда вы будете говорить с врачом, покажите ему полный список лекарств и пищевых добавок, которые вы принимаете, включая витамины и безрецептурные, казалось бы, абсолютно безвредные препараты.
Перед процедурой врач может попросить вас прекратить прием лекарств, которые увеличивают риск кровотечений.
• Антикоагулянты, такие как варфарин (Кумадин).
• Антиагреганты, такие как ацетилсалициловая кислота (Аспирин-Кардио).
• Нестероидные противовоспалительные средства: ибупрофен, диклофенак.
• Диетические добавки, содержащие гинкго двулопастный, рыбий жир, и даже обыкновенный чеснок.
Врач скажет вам, когда следует приостановить прием лекарств, и через какое время после процедуры его можно будет возобновить. Не прекращайте самостоятельно прием препаратов, назначенных вам врачом!
Перед проведением биопсии у вас возьмут образцы крови и мочи, чтобы исключить наличие инфекции и других состояний, при которых проведение биопсии может быть рискованным. Вас могут попросить не есть и не пить за 8 часов до процедуры.
Проведение биопсии
Перед проведением чрескожной биопсии комaнда подготовит вас; они могут ввести вам легкое седативное средство, чтобы помочь расслабиться во время процедуры.
Во время биопсии почки вы будете лежать на животе, ваши почки будут расположены близко к поверхности тела. Если биопсия делается после пересадки почки, то врач скажет вам лечь на спину.
Американские специалисты описывают несколько стадий проведения чрескожной биопсии почек, проведение которых в сумме занимает около 1 часа:
• При помощи ультразвука врач определяет точное место, в которое нужно будет ввести иглу. В некоторых случаях вместо ультразвука используется компьютерная томография.
• Врач помечает на коже место ввода иглы, обpaбатывает кожу и вводит местный анестетик (обезболивающее).
• После подготовки врач делает миниатюрный разрез на коже, через который пройдет игла. Саму иглу вводят под контролем ультразвука.
• Больной делает глубокий вдох и задерживает дыхание, пока врач берет образец ткани, используя специальный инструмент на конце иглы. В этот момент можно услышать тихий щелчок.
• Чтобы взять достаточно ткани, иногда приходится вводить иглу через один и тот же разрез несколько раз.
• После завершения биопсии члeны комaнды накладывают повязку на рану.
Другие процедуры
Чрескожная биопсия почки не является единственным способом проведения этой процедуры. Если у вас имеется история кровотечений, нарушения свертывания крови или только одна работающая почка, то врач может предложить другой метод – лапароскопическую биопсию почки.
В ходе этой процедуры врач делает небольшой разрез, в который вводится видеокамера с подсветкой. Это устройство позволяет вывести на монитор в операционной изображение ваших внутренних органов и аккуратно сделать процедуру.
После проведения биопсии
После чрескожной биопсии почки вам нужно ожидать следующее:
• Некоторое время вы проведете в послеоперационной палате, где персонал будет постоянно следить за вашими жизненными показателями.
• Вам придется лежать спокойно в течение нескольких часов подряд.
• Вам проведут полные анализы мочи и крови, чтобы проверить на наличие кровотечения и других послеоперационных осложнений.
• Вы получите от своего врача инструкции по поводу того, что можно и что нельзя делать в период восстановления.
• После биопсии вы будете ощущать боль в месте укола, поэтому врач выпишет вам aнaльгетики.
Большая часть пациентов может покинуть больницу уже в первый день после биопсии. Возможно, вам понадобится остаться в отделении на 12-24 часа после процедуры, если врач посчитает нужным. Некоторое время вам нельзя будет заниматься интенсивными физическими упражнениями, в том числе поднимать тяжести.
Внимание! Нужно сообщить вашему врачу, если:
• У вас наблюдается значительная примесь крови в моче дольше, чем в течение 24 часов после процедуры.
• Если вы не можете помочиться.
• У вас поднялась температура тела.
• Боль в месте биопсии ухудшилась.
• Вы почувствовали слабость, головокружение.
Результаты биопсии
Образец ткани вашей почки будет отправлен на изучение в лабораторию, где его будет изучать специалист по лабораторной диагностике (в США это патолог). Патолог использует специальные реактивы и красители, которые позволяют увидеть изменения тканей, характерные для той или иной болезни.
Результаты биопсии могут быть готовы через несколько дней. В срочных ситуациях полный или частичный отчет может быть готов уже в первые сутки, в зависимости от возможностей больницы и конкретного случая. Результаты биопсии следует обсуждать только со своим лечащим врачом.
Константин Моканов: магистр фармации и профессиональный медицинский переводчик
Важно знать родителям о здоровье:
FitoSpray для похудения (Фитоспрей)
FitoSpray для похудения ( Фитоспрей) FitoSpray — спрей для похудения Многие мечтают похудеть, стать стройными, обрести фигуру мечты. Неправильное питание,…
08 02 2023 12:44:27
Фитостеролы в продуктах питания
Фитостеролы в продуктах питания Фитостерины Существует много питательных веществ, которые, как утверждают исследователи, могут положительно повлиять на…
07 02 2023 22:26:53
Фитотерапевт
Фитотерапевт Фитотерапевт Я, Ирина Гудаева — травница, массажист, ведущая семинаров по созданию натуральной косметики и курса « Практическое травоведение»…
06 02 2023 7:57:17
Fitvid
Fitvid Брекеты: минусы, трудности, проблемы Брекет-системы помогли избавиться от комплексов миллионам людей. Это действительно эффективный инструмент,…
05 02 2023 4:25:19
Фониатр
Фониатр Фониатрия – один из разделов медицины. Фониатры изучают патологии голоса, методы их лечения, профилактики, а также способы коррекции…
02 02 2023 11:13:50
Форель
Форель Форель относится к отряду лососеобразных, семейству лососевых. Ее тело удлинено, немного сжато с боков, покрыто мелкой чешуей. Замечательной…
01 02 2023 13:14:23
Формула идеального веса
Формула идеального веса Калькулятор нормы веса Вес 65 кг относится к категории Норма для взрослого человека с ростом 170 см . Эта оценка основана на…
29 01 2023 2:19:40
Формулы расчета идеального веса
Формулы расчета идеального веса Фoрмулa «идeальнoго вeса» То, что ожирение шагает семимильными шагами по планете – это факт. И, несмотря на то, что…
28 01 2023 13:37:53
Фосфатида аммонийные соли
Фосфатида аммонийные соли Аммонийные соли фосфатидиловой кислоты ( Е442) Е442 – это пищевая добавка, которую относят к категории эмульгаторов. Вещество…
27 01 2023 12:57:40
Фототерапия новорожденных
Фототерапия новорожденных Фототерапия новорожденных Применение фототерапии для новорожденных С момента своего рождения организм ребенка начинает адаптацию…
26 01 2023 9:36:25
Фототерапия новорожденных при желтухе
Фототерапия новорожденных при желтухе Фототерапия новорожденных После появления ребенка на свет его организм адаптируется к совершенно иным условиям…
25 01 2023 5:54:44
Французская диета
Французская диета Французская диета Эффективность: до 8 кг за 14 дней Сроки: 2 недели Стоимость продуктов: 4000 рублей на 14 дней Общие правила…
24 01 2023 4:18:20
Фрукт Кумкват — что это такое?
Фрукт Кумкват — что это такое? Фрукт Кумкват — что это такое? Впервые упоминают необычный для европейцев фрукт китайские летописи 11 века. Португальские…
23 01 2023 18:37:25
Фруктовая диета
Фруктовая диета Фруктовая диета Эффективность: 2-5 кг за 7 дней Сроки: 3-7 дней Стоимость продуктов: 840-1080 рублей в неделю Общие правила Фруктовая…
21 01 2023 22:44:30
Фруктоза при диабете
Фруктоза при диабете Можно ли фруктозу при сахарном диабете? Для многих диабет является той проблемой, которая вносит в жизнь ряд ограничений. Так, к…
18 01 2023 8:48:42
Фрукт свити – польза и вред
Фрукт свити – польза и вред Свити — что это за фрукт? Что такое свити? Продолжаем разбирать цитрусовые, но как всегда идем не по верхам, а копаем глубже и…
15 01 2023 13:32:27
Фрукты и ягоды
Фрукты и ягоды Разница между фруктом и ягодой Фрукты и ягоды любят практически все. Ведь они такие вкусные и полезные! Мы любуемся лежащими на столе…
14 01 2023 21:23:25
Фтизиатр
Фтизиатр Врачи фтизиатры Москвы Фтизиатр — это дипломированный специалист в области фтизиатрии. Он специализируется на профилактике, диагностике, лечении…
12 01 2023 10:23:40
Фтор в организме человека
Фтор в организме человека Фтор в организме человека Дневная норма потрeбления Мужчины старше 60 лет Женщины старше 60 лет Беременные (2-я половина)…
11 01 2023 23:47:49
Боли в спине после рождения ребёнка
Боли в спине после рождения ребёнка Почему после родов болит спина У мамочек нередко болит спина после родов. Причем, дискомфорт может длиться довольно…
08 01 2023 13:31:50
Фунчоза: польза и вред
Фунчоза: польза и вред Фунчоза: польза и возможный вред Увлечение восточной кухней год от года растет. Принято считать, что такой рацион полезен для…
07 01 2023 16:39:31
Фундук
Фундук В рационе здорового человека обязательно присутствуют орехи в различных вариациях. Среди них выгодно выделяется фундук. Высокая пищевая ценность и…
06 01 2023 7:51:48
Галактоза
Галактоза Галактоза – это представитель класса простых молочных сахаров. В человеческий организм поступает преимущественно в составе молока,…
02 01 2023 20:52:40
Галанга
Галанга С древних времен растения играют важную роль в жизни человека, в том числе и для поддержания здоровья. Некоторые травы известны как лучшие…
01 01 2023 3:12:12
Галега лекарственная
Галега лекарственная Галега лекарственная (Galega officinalis) Син: козлятник лекарственный, козлятник аптечный, козья рута, французская сирень, солодянка…
31 12 2022 0:18:35
Боли в суставах при беременности
Боли в суставах при беременности Боли в суставах при беременности В период беременности у женщины могут возникать различные боли в самых разных местах….
28 12 2022 13:15:17
Гастрит и изжога
Гастрит и изжога Лучшие лекарства от изжоги и гастрита Многие пациенты с гастритом и другими заболеваниями Ж К Т страдают от изжоги. Данный симптом может…
27 12 2022 6:46:38
Где находится ключица у человека на фото?
Где находится ключица у человека на фото? Ключица человека: анатомия, строение, функции Ключица – это единственное костное образование в теле человека,…
24 12 2022 5:58:21