3710 просмотров
12 июля 2021
Добрый вечер, у меня родился сын если считать срок по месячным то роды были 36 недель 4 дня, если считать срок по 1 скринингу то роды прошли на 37 недели и 5 дне. Родился мальчик ростом 52 см и весом 3700г. — 23 июня в 9 вечера.
26 июня в 10 вечера взяли кровь на неонатальный скрининг, через 2 недели пришел результат, в котором было указано:
Адреногенитальный синдром.
17OH = 23,6нмоль/л при норме 17нмоль/л.
Попросили пересдать.
Подскажите что это значит, насколько это может быть опасно?
На сервисе СпросиВрача доступна бесплатная консультация педиатра онлайн по любой волнующей Вас проблеме. Врачи-эксперты оказывают консультации круглосуточно. Задайте свой вопрос и получите ответ сразу же!
Акушер, Гинеколог
Добрый вечер! Этот показатель указывает на генетические рису развития адреногенитального синдрома. Повышение незначительное, поэтому, надо пересдать
Елена, 12 июля 2021
Клиент
Илона, это я и так понимаю, мне это сказали.
Акушер, Гинеколог
Елена, при взятии анализы бывают неправильные результаты. У Вас отличный ребёнок, не переживайте!
Елена, 13 июля 2021
Клиент
Илона, подскажите какие клинические проявления при этом синдроме могут быть. ему сейчас 20 дней. с половыми органами все в порядке. кушает хорошо. стул тоже нормальный. кормлю грудью.
насколько я знаю там есть разные формы тяжелые и не тяжелые как они проявляются?
Акушер, Гинеколог
Елена, добрый вечер! При легкой форме у мальчиков отмечается резкое увеличение полового органа, выраженная пигментация вокруг ануса, половых органов и сосков. При тяжёлой форме диспепсические расстройства (рвота, не связанная с кормлением), понос; обезвоживание (в том числе, вследствие потери жидкости с рвотой и жидким стулом); судороги;
низкое артериальное давление;
нарушения ритма сердца.
Елена, 13 июля 2021
Клиент
Илона, если нет ни каких симптомов а малышу уже 20 дней. Они могут проявиться позже?
Акушер, Гинеколог
При наличии адреногенитального синдрома симптомы могут проявляться сразу, а могут — чуть позже
Елена, 13 июля 2021
Клиент
Илона, если тяжёлая форма то тоже могут позже проявится?
Акушер, Гинеколог
Да. Но Вы прекратите сейчас паниковать и просто спокойно пересдайте анализ!
Елена, 13 июля 2021
Клиент
Илона, если отклонение 17oh превышен не так намного можно определить какая форма синдрома? Анализ я пересдала но результат будет только через 14 дней.
Елена, 13 июля 2021
Клиент
Илона, при тяжёлой форме изменения половых органов тоже присутствует?
Акушер, Гинеколог
Елена, отклонение небольшое и может быть проявлением легкой формы
Акушер, Гинеколог
Елена, 13 июля 2021
Клиент
Сейчас у нас взяли повторный скрининг. А можно сдать какой то анализ отдельно чтобы это проверить побыстрей а не ждать этот скрининг.
Акушер, Гинеколог
Елена, все остальные анализы сдают, начиная с 5 месяцев жизни, сейчас — только скрининг. Понимаете, при любой степени тяжести и форме адреногенитального синдрома (когда он, действительно есть, генетически обусловленный), цифры 17 oh прогестерона увеличиваются в 5-10 раз в сравнении с нормой, а не так, как у ребенка на данный момент
Педиатр
Здравствуйте
Первое, что вам сейчас нужно, это не накручивать себя
При проведении скрининга бывают ошибки, неправильный сбор анализа, нарушена транспортировка, да мало ли что!
Вам необходимо пересдать анализ.
Как сам малыш? Как кушает? Как со стулом?
Родился естественным путем или к/с?
Есть наследственные заболевания в семье?
Елена, 12 июля 2021
Клиент
Дарья, родился естественным путем, кушает хорошо из роддома выписали 3400, сейчас 19 дней малыш весит где то 3870. стул тоже нормальный.
Елена, 12 июля 2021
Клиент
Дарья, насчет наследственных заболеваний я не знаю. у нас с мужем и у родителей нет, ну или не проявлялись.
Педиатр
Половые органы сформированы правильно?
Постарайтесь сейчас не накручивать себя. Малышу нужна спокойная мама. Если бы все было прям совсем плохо, то это проявилось сразу после рождения. А так как вам уже 2 недели и с ребенком все в порядке, то хоть пока патология под вопросом, но не переживайте, это все лечится гормонально заместительной терапией.
У меня на участке было несколько случаев как у вас и слава Богу ни один по итогу не подтвердился.
Елена, 13 июля 2021
Клиент
Дарья, да с половыми органами все вроде в порядке, по крайне мере мне не говорили в роддоме про отклонения, есть небольшое не закрытие крайней плоти, но я так понимаю это к этому не относится
Педиатр
Добрый вечер. Повышен риск адреногенитального синдрома, сказали правильно, нужно сначала переслать и желательно в другой лаборатории.
Педиатр
Елена , здравствуйте. На данном этапе нужно дождаться повторного анализа , возможно что уменьшится до нормы.
Многие длительное время сдают (вплоть до года анализы из пяточки),а после диагноз снимается .
Сказать ,что это не опасно ,я не могу . НО! При вовремя выявленном диагнозе, соблюдении рекомендаций генетика, эндокринолога все корректируется и ребёнок никак и ни в чем не отстаёт от сверстников
Сейчас вы выдохните, запаситесь терпением и пересдайте анализ .
Педиатр, Врач УЗД
Здравствуйте! Колебания в анализе могут быть связаны с гестационным возрастом. Обычно у детей, родившихся раньше срока анализ берут на 7сутки. Но вас, с учетом 37нед, веса и роса, скорей всего написали доношенными. Повторите. Скорей всего придет нормальный анализ, т.к. отклонения незначительные. Будьте здоровы!
Педиатр
Значит что у ребёнка может быть Адреногенитальный синдром (врожденное генетическое заболевание).
Необходимо пересдать для уточнения диагноза.
Оцените, насколько были полезны ответы врачей
Проголосовал 1 человек,
средняя оценка 5
Что делать, если я не нашел ответ на свой вопрос?
Если у Вас похожий или аналогичный вопрос, но Вы не нашли на него ответ — получите свою бесплатную онлайн консультацию врача.
Если Вы хотите получить более подробную консультацию врача и решить проблему быстро и индивидуально — задайте платный вопрос в приватном личном сообщении. Будьте здоровы!
Рекомендованные сообщения
-
- Поделиться
Родила 9 дней назад. Пришел результат неонатального скрининга из пяточки. Подозрение на фенилкетонурию😓 есть тут те кто сталкивался с ложноположительным результатом или у кого детки с такой болезнью? Очень надеюсь, что ошибка, кровь ребёнку брали после еды (смеси). Завтра пересдаём
Ссылка на сообщение
-
- Поделиться
Прошу прощения,уточните А точно ли завтра вам стоит пересдавать.
Пересдают на 21-28 день жизни. В другое время — не инфориамативно.
Ссылка на сообщение
- Автор
-
- Поделиться
@vitleona там праздники и выходные будут, сказали как можно быстрее сдать
Ссылка на сообщение
-
- Поделиться
Мы тоже пересдавали, но там не знаю на какую именно болезнь было подозрение. Врачи не сказали. Звонили когда, что придут перезабор делать — сразу предупредили, чтоб не волновались, что это частое явление.
Но вот к сожалению не могу сказать, каких именно болезней касается
Потом больше никто не звонил. Сыну уже 2.6
Ссылка на сообщение
- Автор
-
- Поделиться
@Эн-оун а вам не сказали из-за чего такие ошибки ?
Ссылка на сообщение
-
- Поделиться
@Katherine1 нет, я вроде не спросила.
Знаю, что иногда неправильно забор делают, там надо соблюдать требования
Ссылка на сообщение
-
- Поделиться
Возможно Вы и супруг носители, можно параллельно провериться и, возможно, исключить вариант
Ссылка на сообщение
-
- Поделиться
@Katherine1 странные. Видимо им пофигу,лишь бы галочку поставить. Протокол неонатального скриннинга будет нарушен.
Через 12 дней- будет 21 число и вы прекрасно успеваете сдать.
Оценивать вас будут по нормам на 21-28 день. А вам по факту 10 дней. Не боитесь, что показательно крови не упал, и вам опять позвонят и будут трепать нервы?
У нас был повышен по муковисцидозу. А сообщили с детской только в 4 месяца, и снова кровь на неонатальный скриннинг рекомендовали сдать. Смешные.
Ссылка на сообщение
- Автор
-
- Поделиться
@vitleona так написано в интернете, что повторно срочно надо сдать
Ссылка на сообщение
-
- Поделиться
2 часа назад, Katherine1 сказал(а):
Родила 9 дней назад. Пришел результат неонатального скрининга из пяточки. Подозрение на фенилкетонурию😓 есть тут те кто сталкивался с ложноположительным результатом или у кого детки с такой болезнью? Очень надеюсь, что ошибка, кровь ребёнку брали после еды (смеси). Завтра пересдаём
У дочки подруги пришёл положительный анализ на врожденный гипотиреоз, с двухнедельный малышкой ездили в область пересдавали, ребенок здоров, но подруга говорит чуть не поседела тогда. Желаю чтобы у вас была ошибка.
Ссылка на сообщение
-
- Поделиться
@Katherine1 тогда возможно только для муковисцидоза сроки ретеста 21-28 день….
Ссылка на сообщение
-
- Поделиться
@Katherine1 Пересдавала с ребенком в месяц. Просто позвонили и сказали надо ещё раз сдать. Врач сказала — может, кружочек плохо был замазан кровью, не полностью. Больше не звонили, ничего не говорили.
Ссылка на сообщение
-
- Поделиться
У нас на муковисцидоз положительный пришел. Сразу пересдавали. Ошибка лаборатории была или забора анализа.
Ссылка на сообщение
-
- Поделиться
3 часа назад, Katherine1 сказал(а):
@Эн-оун а вам не сказали из-за чего такие ошибки ?
Чаще всего не предупреждают, что надо выдержать трехчасовой интервал после еды.
Мне в роддоме сказали не кормить 3 часа, как угодно врямя тянуть, иначе может быть ложноположительный результат.
Ссылка на сообщение
-
- Поделиться
@vitleona здесь важно знать точно прямщас, возможно ребенку нужна специальная смесь. Почти месяц с этой болезнью питаться молоком — просто опасно.
@Katherine1 ошибки в этом тесте не редки, пусть все обойдется.
Ссылка на сообщение
-
- Поделиться
У нас был ложноположительный на муковисцидоз, и у мой соседки по палате тоже. Слава Богу не подтвердилось. Не редкость это, когда ложноположительные приходят, не накручивайте себя заранее. Все будет хорошо!
Ссылка на сообщение
- Автор
-
- Поделиться
Девочки, болезнь подтвердили. Ретест ещё выше чем первый
Ссылка на сообщение
-
- Поделиться
23 минуты назад, Katherine1 сказал(а):
Девочки, болезнь подтвердили. Ретест ещё выше чем первый
Очень жаль, что подтвердили. И хорошо, что так рано. Прогноз благоприятный.
-
1
Ссылка на сообщение
Присоединяйтесь к нашим обсуждениям!
Вы должны быть пользователем, чтобы оставить комментарий

Здравствуйте.
Моему ребенку третья неделя. В роддоме брали у него (почему-то дважды) кровь из пяточки.
Сегодня звонок поступил из детской поликлиники аж в 8 вечера, сын пока не прикреплен даже к больнице. Сказали очень срочно приехать завтра с утра с ребенком — им не нравятся результаты скрининга, хотят перепроверить. На все мои расспросы говорят лишь то, что нужно приехать срочно, а по какой болезни подозрения сказать мне не могут, говорят результаты в понедельник будут и все узнаю.
Прочла про эти 5 болезней. На одну из них, как я понимаю, есть подозрения. Одна страшнее другой, не знаешь даже какое меньшее из зол. В роду от меня и отца никаких патологий во все известные нам поколения не было. Беременная не употребляла спиртное, не курила. Не знаю откуда такие ужасы могли взяться. Реву, переживаю. Завтра видимо тоже ничего не скажут. Как быть до понедельника? С ума сойду.
Подскажите, пожалуйста, может отправляли кого-то на пересдачу анализа? Бывают ли ложноположительные результаты? Может у кого-то положительный результат: какая болезнь, как живете с этим? Не знаю что ищу на форуме. Может ободрения, статистики. Хочу понять к чему готовиться, чего ждать.
Ребенок у меня первый, может паникую много, очень желанный. На вид здоровый (тьфу-тьфу-тьфу). Нет косоглазия даже, адекватный, плачет по нужде (умеренно), доношенный, появился через КС.

Вы выдерживали интервал «голодания» 6 или 4 часа до сдачи?
Я не сдержалась и накормила и именно это дало ложноположительный результат, мед сестра приходила и второй раз на дом тест делать. И всё хорошо в итоге было. Второй раз делали только на ту болезнь, которая дала пограничные результаты.

Я молилась всё время после того,как взяли этот анализ.К сожалению,генетические поломки могут быть у любого ребёнка.Для нас было самое главное,чтобы дети выжили,с остальным всем знали,что справимся.Так и получилось-радуемся каждому дню уже 7лет.Желаю,чтобы у вас всё обошлось и малыш рос абсолютно здоровым.

Milaa_:
Вы выдерживали интервал «голодания» 6 или 4 часа до сдачи?
Нет. Кормила каждые три часа. Мне сейчас из больницы сказали натощак сдавать за 1,5-2 часа после кормления минимум. В роддоме не обратила внимания когда брали, но наверняка предусмотрели. Ребенок на искусственном кормлении, у меня молока нет.
Вам т. е. сообщили на какую болезнь подозрения, долго результат шел? Мне сказали, чтоб до понедельника ждала, но читаю, что 10 дней обычно срок.

Был сомнительный два раза. Пересдавали на Флотской, там же и неонатолог смотрел и генетик. В итоге все хорошо. Был сомнительный по фенилкетонурии.

Все эти болезни излечимы или приглашаются. дети при лечении полноценны. А у вас, может просто не удачный анализ. Поэтому просят пересдать

Аноним:
Желаю,чтобы у вас всё обошлось и малыш рос абсолютно здоровым.
Спасибо Вам!

Автор не паникуйте раньше времени. У нас тоже медсестра приходила на дом и брала кровь на пересдачу. ( и с первым ребёнком и со вторым)…, Со вторым (дочь) вообще чуть с ума не сошла, медсестра проговорилась что плохой анализ на адреногенитальный синдром.
Я когда про этот ужас прочитала в инете, мне так плохо стало что просто жуть. Всё обошлось.
Может это сбой из-за кормления даёт. Они же не предупреждают когда точно в роддоме за анализом протопают, и вот и кормишь ребёночка .

Автор, не паникуйте раньше времени! Даже если что-то не так (т-т-т), мне врач говорила, что для этого и анализ, вовремя выявят — вовремя компенсируют. Смысла в ваших переживаниях нет, забейте. В понедельник будете думать (если вообще будет о чем думать).
Держу за вас кулачки @@@@

Мы со старшим тоже пересдавали этот анализ, я тогда позвонила девочкам, с которыми в роддоме лежали, так оказалось все они пересдавали. В итоге у всех все хорошо.
Я поняла, что часто с этим скринингом проблемы возникают.

Тоже звонили из поликлиники и мы пересдавали этот анализ из пяточки (на муковисцидоз перепроверяли). Ттт, всё обошлось.
Автор, не думайте о плохом раньше времени. Хотя помню свое состояние те 2 недели в ожидании результата. Выдохнула, когда звонок так и не поступил (было сказано, что если плохо все, то позвонят, если нет — нет)

А как передают, если брать анализ надо вроде как строго на 4 или 7 день.
Неонатальный скрининг — это комплекс мероприятий, который дает возможность выявить какие-либо заболевания на доклинической стадии, что позволяет своевременно начать лечение. К сожалению, учитывая большое количество материала, возможны различные ошибки и получение как ложноположительных, так и ложноотрицательных результатов.
Впервые в 1962 году Роберт Маккриди совместно с Робертом Гатри организовали сбор бланков из фильтровальной бумаги с сухими пятнами крови от каждого новорожденного в штате Массачусетт и тестировали их на фенилкетонурию. В настоящее время массовый скрининг новорожденных проводится в 52 странах мира: США — на 45 нозологий, в Германии — 14, Великобритании -5, России -5 (фенилкетонурия, врожденный гипотиреоз, врожденная дисфункция коры надпочечников, галактоземия, муковисцидоз).
Впервые скрининг на врожденный гипотиреоз был проведен в Канаде в 1973 г. путем определения концентрации тироксина (Т4) в капле крови на фильтровальной бумаге радиоиммунологическим методом.
Почему же возникают ошибки при проведению скрининга с целью выявления врожденного гипотиреоза и врожденной дисфункции коры надпочечников (дефицита 21-гидроксилазы)?
Возникновение ошибок при проведении скрининга на врожденный гипотиреоз возможно на всех этапах обследования. Важно учитывать сроки и правила забора крови. Кровь забирается путём чрезкожной пункции (чаще из пятки) на 4-5 день после рождения у доношенных и на 7-14 день у недоношенных детей. Кровью объёмом 6-8 капель полностью пропитывают специальную фильтровальную бумагу.
Возможны ошибки при измерении результатов.
Так же есть ошибки, связанные с нарушением информирования, игнорировании полученных данных.
Существуют варианты гипотиреоза, прикоторых возможно более позднее повышение ТТГ (после взятия скрининговой программы).
Есть варианты гипотиреоза, при которых отсутствует повышение ТТГ (вторичный, резистентность тканей к тиреоидным гормонам).
Ложноположительные результаты могут возникать при ошибке метода. Ложноотрицательные методы — при вторичном гипотиреозе, гипотиреозе, связанном с резистентностью тканей к гормонам щитовидной железы.
В первые недели жизни ребенка заподозрить дефицит 21-гидроксилазы позволяет наличие вирилизации наружных гениталий у девочек и развитие синдрома потери соли у детей обоего пола. Вирильная форма заболевания у мальчиков диагностируется только к 4-5 годам жизни, при появлении симптомов преждевременного полового развития. Костный возраст при этом уже значительно опережает хронологический. Подобный клинический подход к диагностике 21-гидроксилазного дефицита приводит к большому количеству ошибок. До 30% девочек с тяжелыми проявлениями вирилизации наружных гениталий ошибочно регистрируются в мужском поле. До 35% мальчиков с сольтеряющей формой заболевания погибают в первые недели жизни, т.к. заболевание остается нераспознанным.
Своевременно поставить диагноз позволяет неонатальный скрининг на выявление 21-гидроксилазного дефицита, при котором определяется уровень 17 — гидроксипрогестерона. Этот метод был предложен Pung с соавт. в 1977 г. К 1991 г. Программу неонатального скрининга внедрили 29 стран мира.
При заборе крови в роддоме в сопроводительных документах, отсылаемых в лабораторию, помимо стандартной информации необходимо указать вес новорожденного, срок гестации при недоношенности, прием матерью и (или) ребенком дексаметазона, выраженная билирубинемия , применение в/в трансфузии до взятия крови на скрининг.
Выполняется исследование уровня 17ОНП, проводится выборка положительных результатов и повторно тестируются сомнительные результаты. Для детей, рожденных на различных сроках гестации, используются отдельные нормативные стандарты уровня 17ОНП. Это обусловлено тем, что уровень 17ОНП у недоношенных и маловесных детей значительно выше, чем у детей, рожденных в срок и имеющих нормальный вес. Отсутствие нормативной шкалы значений 17ОНР может приводить к большому числу ложноположительных результатов. В лабораториях, осуществляющих скрининг, необходим постоянный контроль качества проведения гормонального исследования. К 9-10 дню жизни доношенного ребенка лабораторная обработка результатов должна быть закончена. Информация о всех положительных результатах должна быть немедленно направлена в поликлинику по месту жительства ребенка или в стационар, где он еще может находиться.
Помимо недоношенности, ложноположительные результаты могут определяться у новорожденных детей с тяжелым общим соматическим состоянием, у детей на фоне в/в трансфузии, у детей с высокой билирубинемией. Ложноотрицательные результаты могут определяться у детей, матери которых (и/или сам ребенок) получали терапию дексаметазоном с целью профилактики и лечения легочной патологии новорожденных (недостаток сульфактана).
Учитывая значительный процент ложноположительных результатов, особенно у недоношенных детей, при отсутствии клинических симптомов следует дважды с интервалом 1-2 недели проводить определение 17ОНП в сыворотке крови, прежде чем начать лечение. Детям с диагностированным адреногенитальным синдромом необходимо проведение молекулярно-генетического исследования для выявления мутаций в гене CYP21. Молекулярно-генетическая диагностика у пациентов с положительным результатом гормонального исследования внедрена в качестве второго этапа скрининга в некоторых странах для уменьшения количества ложноположительных результатов. Проблемой, сдерживающей широкое внедрение данного метода, является его высокая стоимость. Выявление конкретных мутантных аллелей помогает подтвердить диагноз и дифференцировать форму заболевания, что позволяет адекватно подобрать дозы препаратов в периоде новорожденности и раннем детском возрасте. Исследование мутаций в гене СУР21 дает возможность провести дифференциальный диагноз между дефицитом 21-гидроксилазы и 11в-гидроксилазы — гипертонической формой ВДКН, имеющей сходную клиническую картину и сопровождающейся умеренным повышением 17-ОНП. Эффективным методом уточняющей диагностики является анализ стероидного спектра методом жидкостной хроматографии с тандемной масс-спектрометрией, позволяющей оценить уровни 17-ОНП, кортизола и андростендиона. Это дает возможность четко дифференцировать ферментативный дефект при заболевании.
В своей практике не редко приходится сталкиваться с ложноположительными результатами. За время появления скрининговой программы в Крыму по определению дефицита 21-гидроксилазы ложноотрицательных результатов не было.
Несколько отходя от основной темы, но о скрининге. За последние 6 мес. у нас выявлено 3 ребенка с синдромом Дауна. Двоим диагноз поставлен в роддоме. Третьего ребенка с фенотипом синдрома Дауна ко мне на консультацию прислал педиатр с жалобами на большой язык, плохую прибавку в массе, задержку психо-моторного развития. Направила на кариотипирование, результат — 47, ХХ+21. Двое детей от молодых здоровых родителей. Все матери даунят стали на учет на ранних сроках беременности, которые были желанные и запланированные. Соответственно, все скрининговые программы в период беременности проводились.
Поэтому, уважаемые коллеги, если у Вас есть какие-то подозрения, помните, что любой скрининг может выдавать ошибочный результат. Для уточнения диагноза нужно использовать более точные методы исследования.
Литература
1. Петеркова В.А. Врожденная дисфункция коры надпочечников у детей , М., 2003.
2. Дедов И.И., Петеркова В.А. Детская эндокринология., М., 2006
Массовое обследование (скрининг) является самым эффективным способом выявления наиболее распространенных наследственных заболеваний.
Неонатальный скрининг – исследование, проводимое в первые дни жизни ребенка, является самым эффективным способов выявления наследственных заболеваний. Именно неонатальный скрининг позволяет выявить максимальное количество заболеваний еще до появления первых симптомов. Вовремя поставленный диагноз и назначенное лечение, в свою очередь, способны остановить развитие тяжелых проявлений, ведущих к инвалидизации.
Неонатальный скрининг, нередко именуемый в РФ «пяточка», начинается в родильном доме: у каждого новорождённого берется несколько капель крови из пятки на специальный тест-бланк, который направляется в специализированную лабораторию для проведения исследования. Здоровый доношенный новорожденный допускается к скринингу на 2–5 сутки, недоношенный — на седьмой день после рождения.
В Российской Федерации до 2023 г. обязательный массовый неонатальный скрининг предполагал выявление 5 наследственных заболеваний: фенилкетонурии, врожденного гипотиреоза, врожденной дисфункции коры надпочечников, галактоземии и муковисцидоза. В ряде регионов приняты программы по расширению неонатального скрининга до 11-16 заболеваний, однако лучшие зарубежные практики предполагают расширение списка до 50-60 заболеваний.
С 31 декабря 2022 г. вступает в силу приказ №274н «ОБ УТВЕРЖДЕНИИ ПОРЯДКА ОКАЗАНИЯ МЕДИЦИНСКОЙ ПОМОЩИ ПАЦИЕНТАМ С ВРОЖДЕННЫМИ И (ИЛИ) НАСЛЕДСТВЕННЫМИ ЗАБОЛЕВАНИЯМИ», согласно которому неонатальный скрининг на всей территории Российской Федерации расширяется до 36 групп нозологий.
С полным текстом приказа можно ознакомиться по ссылке: http://publication.pravo.gov.ru/Document/View/0001202207130023?ysclid=lbz0767oey298399166
В массовый неонатальный скрининг будут включены дополнительные наследственные болезни обмена (органические ацидурии, нарушения бета-окисления жирных кислот, нарушения цикла мочевины), первичные иммунодефициты, спинально-мышечная атрофия.
В приказе отражены ключевые этапы проведения расширенного неонатального скрининга:
- Для проведения неонатального скрининга на врожденные и (или) наследственные заболевания забор образцов крови осуществляют из пятки новорожденного через 3 часа после кормления, в возрасте 24 — 48 часов жизни у доношенного и на 7 сутки (144 — 168 часов) жизни у недоношенного новорожденного.
- Тест-бланки с образцами крови доставляются из медицинской организации, осуществившей забор образцов крови в медико-генетическую консультацию (центр), которые осуществляют скрининговые лабораторные исследования самостоятельно, либо в течение 24 часов отправляют образцы в медицинскую организацию, способную провести исследование.
- Время проведения скрининговых исследований составляет не более 72 часов от времени поступления тест-бланков с образцами крови в медико-генетические консультации (центры) медицинских организаций.
- Информация о результатах скрининговых исследований передается в медико-генетическую консультацию (центр) субъекта Российской Федерации по месту жительства ребенка.
- При получении результатов скрининговых исследований формируется группа детей «условно здоровых» по всем исследуемым заболеваниям и группам высокого риска врожденных и (или) наследственных заболеваний.
- Дети из группы «условно здоровые» не требуют дополнительных исследований и информирования медицинских организаций о результатах скрининговых исследований.
- В течение 24 часов после получения информации новорожденный из группы высокого риска приглашается в медико-генетическую консультацию (центр) субъекта Российской Федерации для забора образцов крови для повторного скринингового исследования в медико-генетической консультации (центре) субъекта Российской Федерации.
- При наличии медицинских показаний врач-генетик медико-генетической консультации (центра) субъекта Российской Федерации немедленно направляет новорожденного из группы высокого риска на госпитализацию в медицинскую организацию по профилю заболевания, назначает специализированные продукты лечебного питания до получения результатов повторного скринингового исследования и подтверждающей диагностики.
Для реализации программы закупается специализированное оборудование, осуществляется формирование центров для проведения диагностики и дальнейшей маршрутизации пациентов с целью оказания необходимой медицинской помощи.
При наследственных заболеваниях обмена нарушается функция ферментов, участвующих в обмене белков, жиров или углеводов. Поэтому для многих из заболеваний данной группы единственным патогенетическим лечением является диетотерапия, основанная на исключении из рациона патогенетически значимых нутриентов. Полноценного рациона у пациентов, соблюдающих с рождения строгие диетические ограничения, удается добиться за счет специализированных продуктов лечебного питания.
Симптомы наследственных болезней обмена нередко проявляются в первые дни жизни ребенка, а в дальнейшем пациентам необходимо соблюдать пожизненную диету. Это означает, что эффективность лечения вновь выявленных пациентов будет напрямую зависеть от возможности своевременного обеспечения специализированными продуктами лечебного питания.
Ниже представлены ключевые нозологии, выявляемые по программе массового неонатального скрининга с 2023 г., при которых в Российской Федерации зарегистрированы и доступны специализированные продукты производства Nutricia.
Фенилкетонурия
Основу рациона больных ФКУ составляют специализированные продукты, белок в которых замещен полноценной смесью аминокислот за исключением фенилаланина. Остальное меню составляется из низкобелковых продуктов и обычных продуктов со строгим учетом содержания в них фенилаланина.
Диета для пациентов с ФКУ должна начинаться с первых дней жизни и продолжаться пожизненно. Своевременная диагностика и адекватное лечение обеспечивают полноценную жизни пациентов и нормальное умственное развитие. Прекращение или отсутствие диетотерапии приводит к необратимым и тяжелым последствиям, глубокой инвалидизации и сокращению продолжительности жизни.
* Пищевая ценность на 100 г сухой смеси
** Пищевая ценность на 62,5 мл продукта
*** Продукты зарегистрированы на территории государств Таможенного Союза и включены в Перечень специализированных продуктов для детей –инвалидов
Метилмалоновая ацидемия / Пропионовая ацидемия
Основной метод лечения при метилмалоновой и пропионовой ацидемии — соблюдение строгой диеты с ограничением потребления изолейцина, валина, треонина и метионина с пищей. Детям до 6 месяцев материнское молоко и детские молочные смеси полностью заменяют специальным питанием. При введении прикорма с 6 месяцев противопоказаны продукты с высоким содержанием белка: мясо, рыба, яйца, молочные продукты и бобовые.
* Пищевая ценность на 100 г сухой смеси
** Продукты зарегистрированы на территории государств Таможенного Союза и включены в Перечень специализированных продуктов для детей –инвалидов
Глутаровая ацидемия тип I
Лечение заболевания направлено прежде всего на коррекцию метаболических нарушений. Для этого пациенту необходимо подобрать оптимальную диету, исключающую продукты, богатые лизином.
При ранней диагностике и соблюдении режима терапии у 80–90 % пациентов заболевание протекает относительно бессимптомно. При несоблюдении диеты нередко наблюдается прогрессирование развития неврологических симптомов.
* Пищевая ценность на 100 г сухой смеси
** Продукты зарегистрированы на территории государств Таможенного Союза и включены в Перечень специализированных продуктов для детей–инвалидов
Тирозинемия тип I
Основа лечения – диета с назначением смесей, не содержащих тирозин и фенилаланин, т.к. фенилаланин – метаболический предщественник тирозина.
* Пищевая ценность на 100 г сухой смеси
** Продукты зарегистрированы на территории государств Таможенного Союза и включены в Перечень специализированных продуктов для детей–инвалидов
Гомоцистинурия
Пациентам с гомоцистинурией рекомендована диетотерапия с применением специализированных продуктов, не содержащих метионин.
* Пищевая ценность на 100 г сухой смеси
** Продукты зарегистрированы на территории государств Таможенного Союза и включены в Перечень специализированных продуктов для детей–инвалидов
Лейциноз (болезнь кленового сиропа)
Пациентам с лейцинозом рекомендована диетотерапия со строгим ограничением белка, в том числе грудного молока. Дефицит белка восполняется за счет специализированных продуктов, не содержащих лейцин, изолейцин и валин.
* Пищевая ценность на 100 г сухой смеси
** Продукты зарегистрированы на территории государств Таможенного Союза и включены в Перечень специализированных продуктов для детей–инвалидов
Нарушения окисления жирных кислот
Наследственные нарушения окисления жирных кислот — группа наследственных заболеваний, при которых нарушается транспорт жирных кислот в митохондрии и их окисление:
- MCAD — Дефицит ацил-КoA-дегидрогеназы среднецепочечных жирных кислот
- LCHAD – Недостаточность длинноцепочечной З-ОН ацил КоА дегидрогеназы жирных кислот
- VLCAD – Дефицит ацил-КоА дегидрогеназы жирных кислот с очень длинной углеродной цепью
- SCAD — Дефицит ацил-КоА дегидрогеназы жирных кислот с короткой углеродной цепью
- SCHAD — Дефицит короткоцепочечной 3-гидроксиацил- КоА дегидрогеназы
Всем пациентам с VLCAD и LCHAD независимо от возраста необходим индивидуальный рацион, желательно с использованием специализированных смесей с жировым компонентом, представленным среднецепочечными триглицеридами.
* Пищевая ценность на 100 г сухой смеси
** Продукты зарегистрированы на территории государств Таможенного Союза и включены в Перечень специализированных продуктов для детей–инвалидов
Муковисцидоз
Диетотерапия составляет важную часть комплексной терапии при муковисцидозе в связи тем, что установлена непосредственная связь между состоянием питания и функцией легких: существует прямая корреляция между показателем индекса массы тела, функцией легких и продолжительностью жизни.
Основной принцип в организации питания детей и подростков больных муковисцидозом – увеличение энергетической ценности рациона питания за счет увеличения потребления белка в 1,5 раза по сравнению с возрастной нормой и доведения жировой компоненты питания до 40-50% от общей энергетической емкости рациона.
Смеси с повышенной плотностью энергии и питательных веществ (специализированные продукты диетического (лечебного) питания)) имеют лучшее соотношение энергии и белка, более концентрированный профиль питательных микроэлементов. Своевременное назначение диетотерапии и соблюдение режима питания с применением высококалорийных смесей позволяет повысить качество жизни и снизить частоту бронхолегочных осложнений у больных с муковисцидозом.
* Пищевая ценность на 100 мл готового продукта
** Продукты зарегистрированы на территории государств Таможенного Союза и включены в Перечень специализированных продуктов для детей–инвалидов
Реклама
ООО «Нутриция»
Pb3XmBtzszFbRWcs7gwQ7sYpsBYj2PpLK6SDeeU
Пренатальный скрининг на синдром Дауна был введен 20 лет назад без должного общественного и политического обсуждения, что обусловило многие социально-психологические и морально-этические проблемы в здравоохранении и обществе в целом. В ближайшие 5 лет может стать доступна новая технология, поэтому уже сейчас надо развернуть более широкие общественные дебаты по этой теме.
Пренатальный скрининг на синдром Дауна ежегодно охватывает миллионы беременных женщин во всем мире. Его разрешающая способность довольно низка, поэтому в случае положительного результата становится необходимым проведение инвазивных диагностических процедур, связанных с дополнительным риском для еще не родившегося ребенка. Прямым следствием их применения, наряду с выявлением генетических аномалий, является потеря многих детей, которые на самом деле не имели синдрома Дауна.
По нашим оценкам, современная практика скрининга в Англии и Уэльсе ежегодно предотвращает появление на свет примерно 660 детей с синдромом Дауна, но в то же время приводит к потере 400 детей, у которых нет этого синдрома. Хотя пренатальный диагноз стали ставить чаще, он не дает полной гарантии и по-прежнему рождается немало детей с синдромом Дауна (за 15 последних лет отмечен даже 25%-ный рост числа новорожденных с такой хромосомной аномалией).
Качество жизни людей с синдромом Дауна продолжает улучшаться. Во многих странах они стали жить дольше и достигать в жизни большего, чем когда-либо ранее. Количество новорожденных с синдромом Дауна продолжает расти, а средняя продолжительность жизни людей с данным видом генетической аномалии сейчас достигает 60 лет. В соответствии с этим приоритеты в научных исследованиях и практике должны быть сдвинуты с профилактики рождений людей с синдромом Дауна на улучшение медицинской помощи, образования, а также на их поддержку на протяжении всей жизни Мы полагаем, что генетический скрининг на умственные и физические способности должен пройти через широкое публичное обсуждение, прежде чем новые технологии пренатальной диагностики и секвенирования (расшифровки) генома станут доступными широкому кругу пациентов.
Согласно рекомендациям Американского колледжа акушеров и гинекологов, всем беременным женщинам в США должна быть предоставлена возможность пренатального скрининга на сроке беременности до 20 недель с предпочтением скрининга в первом триместре беременности. Ранее Национальный институт клинического мастерства Великобритании (NICE) рекомендовал обеспечить для всех женщины в первом триместре беременности возможность комбинированного тестирования, включая ультразвуковое обследование и анализы крови. В Шотландии недавно было объявлено, что комбинированный тест будет доступен для всех беременных женщин к марту 2011 года.
Пренатальный скрининг нацелен на то, чтобы оценить шансы конкретной женщины на рождение ребенка с синдромом Дауна и помочь родителям принять решение о том, надо ли проводить дополнительные диагностические обследования, которые сопряжены с некоторым риском для еще не родившегося ребенка. Этот процесс становится для большинства пар непростым, т. к. включает значительную долю неопределенности и подвергает испытанию их личностные ценности и установки.
Большинство исследований вплоть до настоящего времени было посвящено анализу точности оценок, получаемых на основе конкурирующих методик скрининга. Вместе с тем явно недостаточно изучено, в какой степени эти процедуры помогают людям принимать осознанное решение и как они влияют на общее благополучие родителей и детей. Проводились лишь отдельные исследования качества жизни людей с синдромом Дауна и тех дополнительных проблем, с которыми им приходится сталкиваться в жизни в связи с их состоянием
Национальный институт клинического мастерства Великобритании в обзоре по этой теме констатирует: «Высокодостоверные данные указывают, что беременные женщины не имеют достаточных знаний для того, чтобы принять осмысленные решения, которые необходимы в отношении скрининга на синдром Дауна». Некоторые специалисты-медики, по-видимому, неправильно понимают результаты тестов скрининга, так что вряд ли стоит удивляться тому, что многим беременным женщинам «особенно трудно осознать, какой смысл заключен в вычислении степени риска».
Кроме того, данные исследований, проведенных в США и Испании, подтверждают предположение, что во многих странах система медицинской помощи и поддержки, предоставляемых людям с данным диагнозом, явно недостаточна.
Консультирование может оказывать отсроченное влияние на качество жизни людей с синдромом Дауна и их близких. Современная практика скрининга потенциально способна отрицательно воздействовать на материнское отношение к ребенку, вызывая страх, пагубный для его развития. Не исключены и нежелательные психологические последствия для некоторых супружеских пар, остановивших свой выбор на селективном прерывании беременности. Эти неблагоприятные эффекты пренатального скрининга не подвергались таким суровым проверкам, как собственно различные его методики.
Гуманитарные и экономические издержки скрининга часто противопоставляются «бремени» и «стрессу», которые накладывает на семью наличие ребенка с синдромом Дауна. Однако исследования, проведенные в семьях, где воспитываются дети с синдромом Дауна, показали, что большинство родителей хорошо справляются с этой ситуацией и связывают с нею не только проблемы, но и позитивные моменты. В исследованиях такого рода обнаружены положительные воздействия на многих сиблингов, растущих в одной семье с ребенком, имеющим синдром Дауна.
Пренатальный скрининг представляет собой обширное поле деятельности для поставщиков соответствующих тестов и вспомогательных услуг. По расчетам специалистов в настоящее время синдром Дауна в Англии и Уэльсе при отсутствии скрининга с синдромом Дауна рождался бы в среднем 1 из 500 живорожденных детей. Потенциальный же рынок для тестов скрининга в Англии и Уэльсе ежегодно составляет почти 700 000 беременностей. Многие биохимические маркеры, используемые при скрининге, подлежат патентованию. И существует обеспокоенность по поводу влияния интересов определенного круга лиц на процесс исследований и формирование политики организаций, предоставляющих услуги и программное обеспечение, связанные со скринингом.
«Сегодня главная движущая сила расширения практики скрининга исходит от медицинских агентств, а не от простых людей и не является результатом демократических дебатов. По поводу скрининга в Великобритании не проводилось парламентских дискуссий и не принималось никаких законов. Политику формулируют консультативные советы, которые выпускают руководящие указания. В медицинской литературе подчеркивается необходимость профилактики страданий и предоставления родителям определенного выбора, связанного с возможностью прервать патологическую беременность. Оказывая давление на общество, органы здравоохранения приводят экономические аргументы: необходимо снизить “пожизненные расходы на медицинскую помощь” людям с синдромом Дауна, избежать дорогостоящих судебных разбирательств по поводу “нежелательного рождения” детей, которым не был поставлен диагноз, и разработать более дешевые, хотя также экономически рентабельные, технологии скрининга»[2]. [ Alderson, P. Prenatal screening, ethics and Down’s syndrome: a literature review // Nursing Ethics. 2001. Vol. 8, № 4. P. 360–-374.]
Итак, каким же образом обстоит дело в современной практике скрининга?
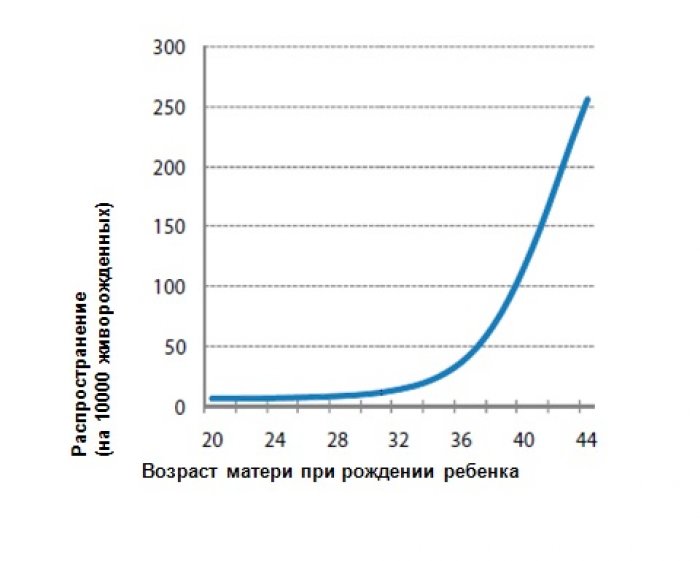
Рис. 1.| Зависимость распространения синдрома Дауна среди новорожденных от возраста матери
Вероятность рождения ребенка с синдромом Дауна увеличивается с возрастом матери, резко повышаясь у женщин старше 30 лет. Следовательно, возраст матери является ключевым фактором, определяющим распространенность синдрома Дауна среди новорожденных в любой конкретной популяции
Теоретическая модель пренатального скрининга
Возраст матери является четким предиктором рождения ребенка с синдромом Дауна (рис. 1). Исторически инвазивную диагностику предлагали матерям старше 35 лет, для которых только фактор возраста уже повышал вероятность рождения ребенка с синдромом Дауна (более чем до 1 на 350 живорожденных детей). Для таких матерей риск рождения ребенка с синдромом Дауна примерно соответствует риску потерять здорового ребенка в результате диагностических процедур. «Логическое обоснование» такого подхода состояло том, что риск рождения ребенка с синдромом Дауна, примерно соответствующий риску потери здорового ребенка или превышающий его, «оправдывает» инвазивные диагностические процедуры.
В 1980-е годы было выявлено, что в крови женщины, вынашивающей ребенка с синдромом Дауна, как правило, имеются определенного рода «маркеры», которые отсутствуют в крови женщин, вынашивающих здоровых детей. Это открытие привело к попыткам улучшить скрининг, основывая его не только на возрастных показаниях, но и на анализе этих «маркеров» в образцах крови матерей. С тех пор в попытках усовершенствовать скрининг беременности на синдром Дауна, сделать его более точным применялись разные комбинации маркеров в сочетании с ультразвуковыми измерениями плода.
Разрешающая способность тестов скрининга такова, что они дают возможность лишь оценить шансы рождения ребенка с синдромом Дауна. Полученные оценки разделяют на «положительные» (высокий риск) и «отрицательные» (низкий риск), причем на основании этих оценок обычно принимают решение о проведении инвазивной пренатальной диагностики. Возможны четыре исхода скрининга: истинноположительный, ложноположительный, истинноотрицательный и ложноотрицательный (рис. 2). Тем матерям, у которых скрининг дал положительный результат, рекомендуют рассмотреть вопрос о проведении пренатальной диагностики инвазивными методами. Поскольку инвазивные процедуры сопряжены с определенным риском прерывания беременности, стратегические установки скрининга направлены на сведение к минимуму ложноположительных результатов. В то же время желательно довести до максимума показатели выявления синдрома.

Рис. 2. | Процесс скрининга, возможные исходы и показатели точности
Степень выявления (доля случаев, когда тесты скрининга позволили точно идентифицировать состояние плода): ИПР / (ИПР + ЛОР) = 85 %. Степень ложноположительных результатов (доля случаев, когда тесты скрининга ошибочно дали положительный результат при отсутствии синдрома Дауна у ребенка): ЛПР / (ЛПР + ИОР) = 6,7 %. Шансы для плода быть фактически пораженным при положительном результате скрининга (ИПР / ЛПР)1 : 20 (цифры иллюстративные)
Таким образом, «граница отсечения риска», то есть рубеж, разделяющий результаты скрининга на положительные и отрицательные, представляет собой, по существу, произвольную величину, балансирующую между степенью выявления синдрома и степенью ложноположительных результатов (рис. 3, а). Более высокая граница отсечения риска уменьшает число ложноположительных результатов, но также снижает и степень выявления (и наоборот), то есть влияет как на число родившихся детей с синдромом Дауна, так и на число потерь здоровых детей (рисунок 3, b). При использовании этой модели предполагается, что процент женщин, которые выбирают инвазивные методы диагностики при положительном результате скрининга, держится на одном и том же уровне и не зависит от вычисленной степени риска.. Но на практике женщины, выбравшие пренатальный скрининг, более склонны к инвазивной диагностике в случае получения повышенной оценки риска.

Рис. 3. | Балансирование между выявлением и ложноположительными результатами при определении границы отсечения риска:
– более высокая степень выявления подразумевает и более высокую вероятность ложноположительных результатов. Равновесие выбирают, устанавливая «границу отсечения», отделяющую результаты с «высоким» риском от результатов с «низким» риском;
– правильное выявление отягощенной беременности имеет место в среднем только в одном из 20–-30 случаев, давших положительный результат при первичном скрининге. Это побуждает многих женщин, беременность у которых фактически не отягощена синдромом Дауна, решиться на процедуры инвазивной диагностики, чреватые возможностью потери здорового ребенка. Выбор границы отсечения – это, по существу, выбор между предупреждением появления на свет больных детей и потерей здоровых детей. (Частотные показатели распространения, выявления и ложноположительных результатов, предсказанные границей отсечения в начале второго триместра беременности и примененные в иллюстративных целях для выборки размером 100 000 беременностей, допускают 60% положительных результатов скрининга, 90% случаев прерывания беременности с синдромом Дауна и 23% случаев естественной потери плода.)
Разница между выявлением и предупреждением
При зачатии у человека необычный численный набор хромосом встречается на удивление часто, по-видимому, затрагивая около 20 % всех оплодотворенных яйцеклеток. Многие такие яйцеклетки теряют жизнеспособность уже на первых неделях беременности. Беременности, отягощенные синдромом Дауна, намного чаще заканчиваются самопроизвольным прерыванием по сравнению с неотягощенными. В публикациях приводятся разные количественные оценки невынашивания беременности. Суммарный показатель свидетельствует о том, что 43 % плодов с синдромом Дауна, диагностированным на сроке беременности от 11 до 13 недель, и 23 % плодов с этим синдромом, диагностированным на сроке от 16 до 18 недель, не доживают до родов. У матерей старшего возраста показатели невынашивания, по-видимому, выше. При отсутствии исследований, проведенных на обширных выборках беременностей, прошедших пренатальную диагностику и прослеженных вплоть до завершения, довольно трудно дать точные числовые оценки. Кажется вполне вероятным, что по сравнению с данными по медицинскому прерыванию беременности или живорождению цифры невыношенных беременностей, фигурирующие в отчетах, часто ниже, чем могли бы быть при отсутствии вмешательств. Беременности, отягощенные синдромом Дауна, не выявленным пренатально (ложноотрицательный результат скрининга), но не закончившиеся рождением живого ребенка, также не включаются в сводки и представляют еще один источник искажения при подсчете данных.
Показатель естественных потерь означает, что количество случаев пренатального выявления синдрома Дауна и медицинского прерывания беременности не соответствуют количеству предупреждений живорождения (поскольку во многих случаях медицинского аборта плод не дожил бы до родов и сам по себе). Показатель естественных потерь также означает, что смещение скрининга на более ранние сроки беременности (например, за счет введения комбинированного теста в первом триместре) позволит выявить больше отягощенных беременностей, при которых плод не выжил бы и без медицинского аборта, то есть во многих случаях искусственное прерывание беременности будет подменять самопроизвольный выкидыш.
Оценки риска для будущих детей
Согласно доступным объективным данным риск прерывания беременности вследствие амниоцентеза составляет 1 %, а вероятность такого исхода после биопсии ворсин хориона (CVS) в первом триместре беременности – около 2 %. Наблюдается выраженная изменчивость по степени осложнений после амниоцентеза под ультразвуковым контролем и после CVS. Исследования выявили, что показатель потерь в результате проведения амниоцентеза в 6–8 раз выше при выполнении процедур начинающими врачами по сравнению с более опытными специалистами.
Ориентация на смещение скрининга в сторону первого триместра беременности (то есть на диагностику через CVS) может существенно увеличить неоправданные потери здоровых детей (без соответствующего снижения доли ложноположительных результатов).
Медицинская практика
Многие опубликованные исследования конкурирующих технологий скрининга моделируют эффекты различных границ отсечения риска. Однако надо признать, что моделирование может оказаться нерепрезентативным в отношении практического осуществления скрининга. Например, прогнозируемая разрешающая способность скрининга с четверным тестом, показанная на рис. 3, при отсечении на уровне ≥1:300 соответствовала степени выявления 86 % и частоте ложноположительных результатов 6,6 %. В то же время проверка разрешающей способности четверного теста в 14 больницах Великобритании показала степень выявления 81 % и частоту ложноположительных результатов 7 % при отсечении риска на уровне ≥1:300. Эти скромные различия соответствуют дополнительной потере двух здоровых детей и уменьшению показателя предупреждения живорождений с синдромом Дауна на 5 случаев в расчете на каждые 100 000 обследованных беременностей.
Другие исследования также наглядно иллюстрируют, насколько реальная практика может могут отличаться от некоторых моделей.
В Великобритании и многих странах Европы пренатальный скрининг в настоящее время доступен для большинства женщин независимо от возраста. В Англии и Уэльсе пренатальный скрининг стал широко использоваться с конца 1980-х годов. Государственный цитогенетический регистр по синдрому Дауна (NDSCR) ведет записи диагнозов и исходов беременности с 1 января 1989 года, а недавно опубликовал данные за 2006 год. Мы проанализировали данные записей NDSCR, чтобы оценить действенность официальных установок по пренатальному скринингу в Англии и Уэльсе за период с 1992 по 2006 год (см. таблицу). NDSCR записывает данные по всем беременностям с диагностированным синдромом Дауна и всем родам в Англии и Уэльсе. Мы сделали поправку на неизвестные исходы, чтобы получить полную оценку случаев живорождения, невынашивания/мертворождения и искусственного прерывания беременности. Затем было оценено число предупрежденных случаев живорождения детей с синдромом Дауна посредством вычитания прогнозируемых естественных потерь из числа беременностей, прерванных искусственно (допуская естественные плодные потери на уровне 43 и 23 % для беременностей, диагностированных через CVS и амниоцентез соответственно).
Записи по исходам тех беременностей, когда по итогам скрининга был получен положительный результат, но диагноз синдрома Дауна не был подтвержден последующими (инвазивными) анализами, не велись. Таким образом, были рассчитаны предположительные потери 45 здоровых детей на каждые 100 случаев пренатального диагноза синдрома Дауна (1 : 2,2) по анализам сыворотки и/или данным ультразвукового обследования, а также потери 143 здоровых детей на каждые 100 случаев синдрома Дауна (1 : 0,7), когда обследование проводилось по показаниям, связанным только с возрастом матери. Для введения поправки на возможные усовершенствования в практике, связанные с более частым в последние годы применением комбинированного теста, мы допускаем, что в период с 2001 по 2006 год потери здоровых детей снизились до 31 случая на каждые 100 беременностей с пренатальным диагнозом синдрома Дауна, поставленным по анализам сыворотки и/или результатам ультразвукового обследования (1 : 3,2). Эти допущения были приняты на основе данных о частоте выявления синдрома Дауна и доле ложноположительных результатов с применением четверного скрининга в практической работе 14 больниц Великобритании (46 000 беременностей, в том числе 88 с синдромом Дауна), о прогнозируемых рабочих характеристиках скрининга по возрасту матерей в том же исследовании, а также по данным, полученным при комбинированном скрининге в исследовании с участием 15 медицинских центров в США (36 000 беременностей, в том числе 92 с синдромом Дауна). Оценивая эти потери, мы исходили из допущения о частоте потерь в результате инвазивных диагностических процедур (CVS или амниоцентеза) порядка 1 %.
Оценочные характеристики пренатального скрининга по Англии и Уэльсу за период 1991–2006 гг.[3] [Данные за 2006 г. носят предварительный характер]
Трудно сказать, насколько точно эти допущения отражают положение дел в современной практике за отчетный период. Точные данные об использованных тестах скрининга и решении матерей после положительного результата скрининга не записывались (хотя NDSCR недавно начал сбор данных о тестах скрининга). Принятие этих допущений было основано на показателях, наблюдаемых в практике при проведении наиболее эффективного (четверного) теста по крови. В то же время следует отметить, что в отчетный период широко использовались двойной и тройной тесты, обладающие меньшей разрешающей способностью. Ультразвуковой скрининг без анализа маркеров крови также обладает худшими характеристиками по сравнению с четверным скринингом.
Таким образом, возможна следующая трактовка результатов современных наблюдений. Во-первых, хотя политика в области здравоохранения пропагандирует пренатальный скрининг в целях селективного прерывания беременности, сейчас рождается больше детей с синдромом Дауна, чем 15 лет назад, в том числе в процентном отношении к общему количеству новорожденных (рис. 4). За этот период оценочное снижение живорождений детей с синдромом Дауна за счет политики массового скрининга составило 44 % (с 16 985 при отсутствии вмешательств до 9525). Без скрининга у родителей могли бы быть разные соображения относительно сохранения беременности, но, тем не менее, интересно отметить, что со сдвигом деторождения на более поздний возраст связан ожидаемый рост распространения синдрома Дауна среди живорожденных без вмешательств, исходя из оценочной цифры 50 % (увеличение с 14,0 до 21,8 на 10 000) в период с 1992 до 2006 г.
Рис. 4 | Число живых детей, рождающихся с синдромом Дауна, продолжает расти:
а – общий показатель живорождений достиг пика за последние 15 лет, несмотря на приблизительно трехкратное увеличение числа пренатально диагностированных случаев этого синдрома;
б – распространение среди живорожденных продолжает увеличиваться, поскольку деторождение происходит в более позднем возрасте. При отсутствии прерываний беременности по показаниям, связанным с пренатальным диагнозом синдрома Дауна, его распространение среди живорожденных в настоящее время можно было бы оценить на приблизительном уровне 22 : 10 000 (1 : 455). Эти цифры примерно соответствуют современным данным о распространении синдрома Дауна среди новорожденных в Ирландии (где аборты запрещены законом).
Мы делаем вывод о том, что современная политика скрининга, по-видимому, ежегодно снижает число живорожденных детей с синдромом Дауна в Англии и Уэльсе приблизительно на 660 новых случаев и одновременно ведет к потере 400 детей, у которых нет синдрома Дауна. Введение обязательного комбинированного скрининга в первом триместре (как это рекомендовано Национальным институтом клинического мастерства Великобритании, Американским колледжем акушеров и гинекологов и недавно принято в Шотландии) приведет к выявлению большего числа детей с синдромом Дауна, которые в естественных условиях не дожили бы до родов. Если на практике вероятность потерь после CVS выше, чем после амниоцентеза, то принятие комбинированного скрининга в первом триместре может увеличить потери детей, у которых нет синдрома Дауна.
Жизнь по праву
Качество жизни большинства людей с синдромом Дауна во многих экономически развитых странах за последние 40 лет значительно улучшилось, существенно изменилась поддержка этих людей со стороны общества. Их медицинские потребности по большей части поняты обществом и удовлетворяются. Хорошая медицинская помощь помогла увеличить среднюю ожидаемую продолжительность жизни людей с синдромом Дауна во многих развитых странах приблизительно до 60 лет (с 12 лет в 1949 году), и все большее число таких людей сейчас реально доживает до возраста старше 70 лет. Растет число молодых людей с синдромом Дауна, получивших доступ к эффективному образованию и лечению, благодаря чему они достигают более высокого уровня грамотности и навыков общения. Все больше взрослых людей с синдромом Дауна, которые имеют общественно полезную и хорошо оплачиваемую работу, а также достигают достаточно высокого уровня контроля над своей жизнью. Предстоит еще многое сделать, и в отношении этого важного меньшинства людей пока остается много нерешенных проблем, но прогресс, достигнутый людьми с синдромом Дауна, поистине впечатляет.
Прогнозирование качества жизни
Знание того, что кто-то имеет не 46, а 47 хромосом, еще не дает достаточных оснований для точного предсказания качества его жизни. Одни дети с синдромом Дауна рождаются с пороками сердца (около 44 %), а у других таких врожденных пороков развития нет, у одних взрослых развивается деменция (до 9 % в возрасте 49 лет, до 18 % в возрасте 50–54 и до 35 % в возрасте 55–59 лет), а у других она не развивается, одни дети обучаются с большими трудностями, а другие достаточно легко, хотя число хромосом у всех людей с синдромом Дауна совершенно одинаковое. Парадоксально, но синдром Дауна, по-видимому, дает защиту от некоторых раковых и сердечно-сосудистых заболеваний.
Некоторые люди с синдромом Дауна пишут книги, снимаются в кино и на телевидении, среди них есть компетентные музыканты и талантливые спортсмены. Однако другие люди с синдромом Дауна с большим трудом находят себе применение в профессиональной сфере, поскольку могут выполнять только работу низкой квалификации. Многие люди с синдромом Дауна способны вносить позитивный вклад в семейные и общественные отношения, нередко создавая в жизни прочные связи на основе преданности и заботы. Очень редко таким людям свойственно антиобщественное, насильственное или криминальное поведение.
Качество жизни и общество
Насколько нам известно, до сих пор не проводилось серьезных и масштабных исследований, посвященных взглядам людей с синдромом Дауна на качество их жизни. В порядке наблюдения можно отметить, что они не рассматривают свое физическое и умственное состояние как источник страданий. Качество жизни людей с синдромом Дауна во многом зависит от отношения к ним общества, а не от синдрома Дауна как такового.
Надо ли продолжать скрининг?
Авторы этой статьи не считают синдром Дауна достаточным основанием для прерывания беременности и поэтому не согласны с основной идейной предпосылкой скрининга на синдром Дауна. Более того, потери детей, не имеющих синдрома Дауна, которые неизбежны в этом процессе, представляются неоправданными. И эта обеспокоенность довольно широко распространена в кругах специалистов. Обзорный анализ 40 случайно отобранных комиссий по этике научных исследований показал, что 86 % экспертов не считают современную практику скрининга и сопряженный с ней риск этически приемлемыми для достижения главной цели – избежать рождения человека с синдромом Дауна.
Будущее
Политика в области здравоохранения, связанная с селективным прерыванием беременности, в настоящее время не нацелена на большинство других генетических причин интеллектуальных нарушений, или поддающихся лечению болезней
Идет интенсивный поиск способов надежного выделения плодной ДНК из образцов материнской крови. В то же время есть еще одна насущная задача, требующая решения, – это снижение стоимости секвенирования генома хотя бы до 1000 долларов. Когда в обоих этих направлениях произойдет существенный сдвиг, мы сможем дать будущим родителям всестороннюю информацию о значительных факторах риска и множестве возможных исходов, которые могут повлиять (но могут и не повлиять) на качество жизни.ребенка.
«Если ДНК плода можно будет получать неинвазивно, то в практике скрининга мы создадим огромный массив информации с неопределенным значением. Такая информация способна принести больше вреда, чем пользы…» [3] [Shuster, E. Microarray genetic screening: a prenatal roadblock for life? // The Lancet. 2007. № 369(9560). P. 526–-529.]
Как могут супружеские пары придти к осознанному решению, сталкиваясь (например) лицом к лицу с выбором между оценочным уровнем риска аутизма и деменции? Как много беременностей может быть отвергнуто супружескими парами в стремлении получить «наилучшего» ребенка? Какое влияние окажет подобная практика на людей, которые «проскользнули через сито» и родились с «нежелательными» признаками?
Пренатальный скрининг на синдром Дауна был введен 20 лет назад с недостаточным общественным и политическим обсуждением. Когда станет реальным и широко доступным скрининг всего генома, многие неприятные проблемы, возникшие в результате опыта, полученного при скрининге на синдром Дауна, еще больше обострятся. Новая технология может стать доступной для нас в ближайшие 5 лет, поэтому уже сейчас надо развернуть более широкие общественные дебаты по этой теме.
Взгляды, выраженные в этой статье, отражают мнение ее авторов, которое не обязательно совпадает с личным мнением всех членов редколлегии.
Перевод А. Н. Прыткова
Скрининг в период новорожденности — это массовое обследование детей, практикуемое не только в нашей стране, но и в странах Европы и Америки. Обычно его еще называют «пяточным» тестом и проводят для всех детей, рожденных в любых учреждениях родовспоможения. Необходимость данного скрининга продиктована ростом заболеваемости тяжелыми, но вполне поддающимися коррекции в раннем возрасте заболеваниями у младенцев. Сегодня в число болезней, которые выявляет скрининг, относят пять серьезных патологий.
Скрининг новорожденного — что это и зачем?
Такой анализ выполняется всем детям без исключений в период 4-5 суток (либо, по показаниям, и позднее). Результат этого скрининга будут получены позднее, через три-четыре недели, уже в поликлинике, если выявлены те или иные отклонения. Переживать по поводу проведения подобного исследования не стоит — это нужное и важное мероприятие. По мнению докторов, скрининг новорожденного относится к наиболее эффективным мерам ранней диагностики генетических и обменных патологий в раннем возрасте, когда еще можно начать коррекцию и сохранить малышу здоровье. Данный скрининг новорожденного рекомендован к массовому проведению ВОЗ и внедрен во многих странах как обязательное и бесплатное для родителей исследование. Наша страна практикует подобное исследование уже более 15 лет, и его результаты позволили вовремя выявить детей с проблемами и оказать им квалифицированную помощь, не допуская серьезных осложнений.
Проведение скрининга у детей
У нас в стране проводится скрининг пяти самых серьезных и тяжелых патологий, другие страны практикуют выявление до 40 различных патологий. Если ребёнок относится к группе риска и родители хотят провести дополнительное обследование (оно платное), скрининг можно расширить до 16 возможных патологий. Возникает вопрос, почему именно пять патологий? В списке исследуемых находятся те болезни, которые при раннем их выявлении, поддаются лечению, или степень их тяжести может быть значительно уменьшена. В основном, это болезни обмена, а вот хромосомные аномалии сюда не включены.
Забор крови для анализа проводится по строгим срокам — дети, рожденные доношенными, обследуются на 4-5 сутки, для недоношенных сроки сдвигают позже 7 дня. При выписке новорожденного ранее этого срока, забор крови для анализа проводится на дому или в условиях поликлиники, за которой закрепили малыша. Исследуют капиллярную кровь, взятую из пяточки, отсюда и название метода. Капельки крови наносят по особым методикам на пять круглых бланков с особой фильтровальной бумагой. Важно, чтобы анализ был взят натощак, примерно 3 часа до забора ребёнка не кормят.
Важно, чтобы сроки скрининга были соблюдены. Дети, которым анализ взят ранее (на 1-3 сутки жизни), могут давать ложные результаты (как положительные, так и отрицательные). Но и позже 10 суток кровь забирать нежелательно, это затянет получение результата, для многих из выявляемых патологий ценным будет буквально каждый день.
Что может выявить скрининг новорожденного
Первое, что может выявить скрининг новорожденного, это состояние врожденного гипотиреоза (резко подавленные функции щитовидной железы). Если вовремя не начать терапию, последствия этой патологии серьезны — задержка как физического роста и развития, так и сильная психическая отсталость, вплоть до кретинизма. Встречается с частотой 1:5000 новорожденных, при своевременном выявлении дети имеют шансы на полную коррекцию патологии. Конечно, потребуется практически пожизненный прием замещающих гормонов, но это позволит детям расти и развиваться полноценно как физически, так и умственно.
Помимо этого, скрининг новорожденного помогает в выявлении муковисцидоза. Это генетическая патология, приводящая к нарушению секреции желез дыхательной и пищеварительной систем. Встречается у 1 из 3000 детей, при раннем начале заболевания, дети имеют благоприятные прогнозы для жизни и здоровья при условии адекватной терапии.
Реже выявляют адреногенитальный синдром (1:15тыс), но он проявляет себя нарушением выработки у детей гормонов корой надпочечников. Это существенно влияет на развитие органов и тканей, работу сердца. Патология без адекватной терапии смертельно опасна, лечение будет заключаться в пожизненном приеме препаратов.
Еще две патологии, которыми могут страдать дети, и которые выявляет скрининг — это галактоземия и фенилкетонурия. Это генетические заболевания, при которых страдает выработка особых ферментов, участвующих в метаболизме. Они приводят к тяжелым и необратимым последствиям, если своевременно их не выявить. Лечением подобных проблем будет пожизненная диета с исключением галактозы или фенилаланина.
Вопросы по результатам скрининга
Вокруг данного анализа существует много споров, и те родители, у кого результаты скрининга оказались ложно-положительными, пережили множество тяжелых минут. Но те, кому данный скрининг дал своевременные данные о болезни ребёнка, ему благодарны. Дети получили лечение своевременно, что позволило им сохранить здоровье и полноценно развиваться. Поэтому, важно знать ответы на основные вопросы, кающиеся данного обследования. И прежде всего, как узнать результаты скрининга. Готовится анализ до трех недель, поэтому, если в месячном возрасте на приеме педиатр вам ничего не сообщил, значит, результаты отрицательны. Если же результаты положительны — это ее не диагноз, но вам сообщат из клиники, что необходимо прохождение повторных анализов и углубленного обследования. Иногда бывают ложно-положительные результаты (особенно в случае муковисцидоза).
Если повторно выявлены позитивные результаты скрининга, необходимо посещение генетика и направление на обследование к врачам-специалистам и более прицельные анализы. После подтверждения диагноза, производится немедленное принятие решения о лечении крохи.
Насколько результаты скрининга достоверны, но могут ли они не показать болезнь? Если анализ взят правильно, натощак, то его результаты достаточно достоверны. Но это еще не диагноз. Кроме того, в редких случаях бывает так, что при отрицательном результате заболевание есть, и оно выявится уже позднее, при наличии первых симптомов.
Педиатрия. Национальное руководство / под ред. А. А. Баранова – 2014
Неонатальный скрининг новорожденных ХМАО в 1999-2003 гг / Кунцевич Н.В., Белошицкая Т.А., Урванцева И.А. // Медицинская генетика – 2005 – Т. 4 №5
Аудиологический скрининг новорожденных / Шилова Н.А., Харламова Н.В., Чаша Т.В., Толкачева Е.В. // Вопросы практической педиатрии – 2009 – Т. 4 №S1
Что такое пренатальный скрининг?
– Пренатальный скрининг – это комплекс исследований, которые проводят женщине во время беременности. Он включает в себя УЗИ, сбор анамнеза, измерение веса, роста, артериального давления и анализы крови на биохимию и гормоны. Скрининг помогает выявить врожденные аномалии плода и предотвратить развитие осложнений беременности.
Скрининг в дословном переводе означает просеивание. Задача врачей – из большого числа беременных женщин выявить пациенток с высоким риском генетических отклонений плода или осложнений беременности.
Изначально скрининг первого триместра был задуман для выявления синдрома Дауна. Но сейчас задачи и возможности значительно расширились: уже в 11-14 недель в ходе исследования можно получить большой массив информации, чтобы благополучно, с минимальными рисками вести беременность. Например, на раннем этапе можно прогнозировать риск преэклампсии, которая является одним из факторов преждевременных родов, и назначить профилактическое лечение.
Какие патологии позволяет выявить скрининг?
– Со стороны плода в первом триместре благодаря совершенствованию ультразвуковых аппаратов можно выявить большое количество пороков развития: не только грубые, например, анэнцефалию – отсутствие головного мозга. А при оценке маркеров хромосомных аномалий (воротниковое пространство, носовая кость, венозный проток, кровоток на трикуспидальном клапане – клапане между правым предсердием и правым желудочком сердца) заподозрить синдром Дауна, Эдвардса, Патау и другие заболевания.
Также скрининг позволяет диагностировать большие акушерские синдромы – преэклампсию, синдром задержки роста плода. На основании анамнеза пациентки и оценки шейки матки мы можем говорить о риске преждевременных родов. Во время скрининга врач обязательно осматривает придатки матки, яичники: иногда впервые во время беременности у пациенток обнаруживается какой-то онкологический процесс, который требует немедленного лечения.
Многие женщины боятся ошибок диагностики (бывает, врачи говорят, что ребенок родится с синдромом Дауна, но позже выясняется, что все ок). Насколько высока эта вероятность? И можно ли избежать ошибок?
– Вопрос сложный. Ошибки, конечно, случаются и в отношении ранней диагностики. Маркеры хромосомных аномалий – не равно 100% наличие синдрома. Это лишь говорит о том, что у пациентки повышен риск по сравнению с другими женщинами, у которых эти показатели в норме. Это повод дополнительно обследовать пациентку и своевременно выявить те или иные проблемы.
К тому же, в рамках скрининга первого триместра ряд анатомических структур плода остается за кадром: например, однозначно сказать про пороки сердца на этом сроке мы не можем. Это не ошибка, но ограничение метода: мы можем что-то заподозрить или наоборот не увидеть проблему, которая будет выявлена позже.
Бояться скрининга, потому что могут что-то найти – неправильно. Я сторонник того, что пациент должен иметь максимум информации о себе, и эта информация должна быть максимально объективной. Но если врачи что-то обнаружили, женщина всегда может пойти к другому специалисту и перепроверить.
Некоторые женщины решают не проходить скрининг, так как уверены, что не будут прерывать беременность, даже если у плода найдут аномалии…
– Здесь не стоит вопрос о прерывании. Сейчас действительно большое количество пациенток даже в случае подтвержденных генетических синдромов оставляют беременность – это выбор и право родителей.
Речь о том, что есть пороки развития, которые можно прооперировать во время беременности, на очень ранних сроках, и помочь малышу. Например, обструкция мочевыводящих путей – когда на уровне мочевого пузыря происходит нарушение оттока мочи. Выполнив операцию до 16 недели беременности, мы можем сохранить ребенку функцию почек. Если этот момент упускается, к сожалению, запускаются процессы разрушения структуры почки – и ребенок рождается с почечной недостаточностью.
Поэтому УЗИ и скрининги дают дополнительный шанс: чем раньше мы начнем лечение, тем лучше исходы. Есть целый комплекс проблем, которые успешно решает фетальная хирургия (то есть хирургия плода) – это лечение синдромов фето-фетальной трансфузии, обратно-артериальной перфузии, синдрома анемии и полицитемии, врожденной диафрагмальной грыжи, крестцово-копчиковой тератомы, а также таких тяжелых врожденных пороков, как спинномозговая грыжа (Spina bifida). Все эти пороки можно прооперировать, когда ребенок находится еще в утробе.
Может ли УЗИ негативно влиять на ребенка?
– Если бы ультразвук имел какое-то патологическое или вредное воздействие, его бы уже давно запретили или как-то ограничили. Ультразвуковые исследования в акушерстве и гинекологии используются в нашей стране с 1970-х годов. Уже несколько поколений детей выросло с тех времен, и нельзя сказать, что с ними что-то не так.
Сейчас ультразвуковые системы еще более совершенны, и настройки в них максимально оптимизированы для использования в акушерстве. Есть нюансы: например, не рекомендуется применять допплерометрию до 10 недель беременности, поэтому мы не даем послушать сердечко на ранних сроках – мы показываем, что оно бьется, с помощью других режимов. В целом УЗИ не оказывает никакого патологического влияния на плод.
Сколько раз во время беременности и в какие сроки женщина проходит скрининг?
– Ранее в рекомендациях Минздрава было прописано три обязательных скрининга:
- первый – на сроке с 11 недели по 13 недель и 6 дней
- второй – с 19 недели по 21 неделю беременности
- третий – с 30 по 34 неделю беременности.
К сожалению, в последнем приказе от 20.10.2020 № 1130Н остались обязательными только первые два скрининга. Я считаю это упущением: третий скрининг давал нам много информации не только о пороках, которые поздно проявляются, но и, что важнее – давал оценку роста плода. Ранняя задержка роста плода возникает редко, большинство задержек проявляется ближе к 30 неделям. Также мы можем выявить ряд пороков развития, которые потребуют лечения после рождения.
Что делать, если женщина не может пройти скрининг в указанные сроки? Есть ли смысл обследоваться позже?
– Что касается второго скрининга, не принципиально, если пациент придет в 22-23 недели: здесь привязка ко времени объясняется тем, что в случае выявления грубого порока развития, до 22 недель врачи смогут провести прерывание беременности в обычном роддоме. Если же порок выявляется в более позднем сроке, аборт по медицинским показаниям будет возможен только в специализированных перинатальных центрах.
С первым скринингом все несколько сложнее: параметры воротникового пространства мы можем оценивать только в сроках от 11 недели до 13 недель и 6 дней, и при копчико-теменном размере эмбриона от 45 до 84 мм. Если будущий человек из этих диапазонов выпадает, то программа не рассчитывает риск отклонений – так заложена математическая модель. Такие случаи происходят, когда пациентка обращается для прохождения скрининга слишком рано либо слишком поздно.
Когда оправдано дополнительное назначение ультразвуков между обязательными скринингами?
– Есть ряд показаний, и их достаточно много, когда мы выходим за рамки трех стандартных исследований. Это и задержка роста плода, и наличие у пациентки резус-конфликта, когда мы можем выявлять анемию плода или гемолитическую болезнь, и там количество исследований после 30 недель может быть еженедельным и раз в 2 недели после 20 недель. То же касается и двоен, в первую очередь монохориальных, когда развитие осложнений бывает настолько быстрое, что пациентов необходимо наблюдать каждые 2 недели, начиная с 16 недель.
Это пациентки с риском преждевременных родов, у которых преждевременные роды были в анамнезе: мы оцениваем шейку в первом триместре, во втором триместре, и дальше уже по ситуации. Если у врача возникают какие-то сомнения после осмотра на кресле руками, пациентку направляют на трансвагинальное УЗИ.
Также, это пациенты групп риска по преэклампсии – мы должны смотреть, как ребенок растет, нет ли задержки роста, оценивать показатели кровотока при помощи допплерометрии.
Большинство беременных из мегаполисов на самом деле проходят за беременность более трех исследований.
Чем отличаются ультразвуковые исследования 2D и 3D? И какой тип лучше для первого скрининга?
– Весь ультразвук начинается с обычного 2D исследования, этот режим позволяет в полной мере оценить состояние пациента. Трехмерное (то, что называется 3D) для нас, специалистов по визуальной диагностике, не дает какой-то дополнительной информации, но позволяет сохранить большой объем данных в небольшом файле. 3D для пациента позволяет на больших сроках показать, как растет малыш, его лицо, конечности. Но если мы не сделали красивую картинку эмбриона или плода, это не значит, что мы не сделали 3D.
*Статья подготовлена с использованием гранта Президента Российской Федерации, предоставленного Фондом президентских грантов.
Беседовала Алена Демина